
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| ① | 用激光笔照射甲组制得的PAC溶液 | 光亮的通路 | |
| ② | 取乙组制得的样品少许加入铝试剂阿罗明拿 | 变成玫瑰红色 | |
| ③ | 取丙组样品少许,溶于适量的水制得的淡黄色透明液体中加入氟化铵 |
| m |
| M |
| ng |
| 102g/mol |
| ng |
| 102g/mol |
| 9n |
| 17 |
| 9n |
| 17m |
| 9n |
| 17m |


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
A、
| ||
| B、聚合氯化铝{[Al2(OH)nCl2]m}中,n=4 | ||
| C、用电子式表示CaH2的形成过程:H?+?Ca?+?H→H:Ca:H | ||
| D、0.1mol NH3中含有的N-H键的数日为0.3NA(NA表示阿伏加德罗常数的数值) |
查看答案和解析>>
科目:高中化学 来源: 题型:
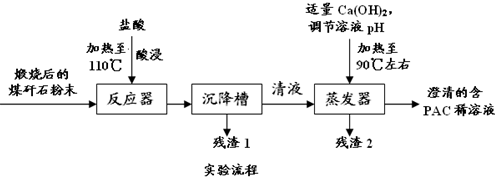
查看答案和解析>>
科目:高中化学 来源:山东省青州一中2012届高三化学一轮跟踪训练:第3章 第2讲 硅 无机非金属材料(鲁科版) 鲁科版 题型:058
| |||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 1.1水的净化与污水处理练习卷(解析版) 题型:选择题
聚合氯化铝(PAC)通式为[Al2(OH)nCl6-n]m,是无机高分子混凝剂,它是用软铝矿(主要成分Al2O3·H2O)为原料制备,制备的最后一步反应是将Al(OH)3凝胶与[Al(OH)2(H2O)4]Cl按照一定配比恰好完全反应制得PAC,则该反应中前者与后者的物质的量之比为( )
A.1∶1 B. 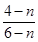
C. 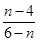 D.
D. 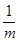
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com