
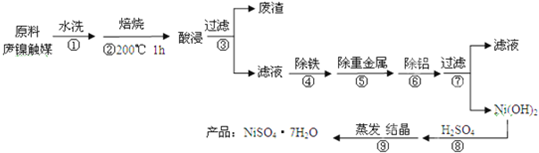
| ԭ�������� m/g | ˮ���� V��H2O��/ml | �������� V��H2SO4��/ml | ������ m��Ni��/g | ������ E��Ni��/% |
| 100 | 200 | 10 | 11.40 | 87.69 |
| 100 | 200 | 20 | 11.60 | 89.23 |
| 100 | 200 | 50 | 11.65 | 89.62 |
| 100 | 200 | 100 | 11.66 | 89.69 |
| 100 | 200 | 150 | 11.68 | 89.85 |
| 59 |
| 281 |
| 11.8 |
| 100��13.0% |
| 59 |
| 281 |
| 11.8 |
| 100��13.0% |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3��8 | B��1��4 |
| C��2��5 | D��4��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
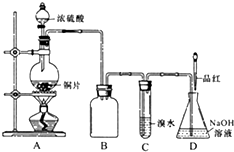 ij��ѧ��ȤС�����ʵ�飬��Ũ������ͭ��Ӧ�Ƶ�SO2���������ʵ��̽����
ij��ѧ��ȤС�����ʵ�飬��Ũ������ͭ��Ӧ�Ƶ�SO2���������ʵ��̽����| ʵ����� | ʵ����� | ���� | ��Ӧ�Ŀ������ |
| �� | �μ��������۵⻯����Һ���� | �� | |
| �� | �μ������غ�ɫ��KI3��Һ���� | �� | |
| �� | �������������KMnO4��Һ���� | ��Һ����ɫ | |
| �� | ���뼸С��CaCO3���� | �����ݲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
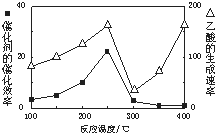 CH4��CO2��Ӧ���������ֵ���ߵĻ�ѧ��Ʒ��
CH4��CO2��Ӧ���������ֵ���ߵĻ�ѧ��Ʒ��| �� �� | CH4 | CO2 | CO | H2 |
| ƽ��Ũ�ȣ�mol?L-1�� | 0.5 | 0.5 | 2.0 | 2.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ƽ��������Ӧ�����ƶ� |
| B��a��c+d |
| C��D������������ |
| D��A��ת���ʱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | A | B | C | D |
| ���� | Ũ���� | �ƾ� | С�մ� | ����� |
| ��ʶ |  |  |  |  |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� | C���٢� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ӻ������п��ܺ��й��ۼ� |
| B�����Է����в����зǼ��Լ� |
| C���Ǽ��Է���һ�������зǼ��Լ� |
| D�����ۻ������п��ܺ��к������Ӽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com