
°æƒø°ø25°Ê°¢101kPaœ¬£¨œ°«øÀ·”Îœ°«øºÓ»Ð“∫∑¥”¶÷–∫Õ»»Œ™57.3kJ/mol°£
£®1£©–¥≥ˆ±Ì 朰H2SO4”Îœ°…’ºÓ»Ð“∫∑¥”¶µƒ÷–∫Õ»»µƒ»»ªØ—ß∑Ω≥Ã Ω£∫___°£
£®2£©—ß…˙º◊”√50mL0.25mol/L¡ÚÀ·”Î50mL0.55mol/L…’ºÓ»Ð“∫≤‚∂®÷–∫Õ»»◊∞÷√»ÁÕº°£
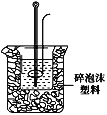
¢Ÿ µ—È ±À˘–˵ƒ≤£¡ß“«∆˜≥˝…’±≠°¢¡øÕ≤Õ‚ªπ–Ë£∫__°£
¢⁄∏√◊∞÷√÷–”–“ª¥¶¥ÌŒÛ «£∫___°£»Áπ˚”√∏√¥ÌŒÛ◊∞÷√≤‚∂®£¨≤‚µ√µƒ÷–∫Õ»»¶§Hª·___(ÃÓ°∞∆´¥Û°¢∆´–°°¢ŒÞ”∞œÏ°±)°£
¢€»Áπ˚”√60mL0.25mol/L¡ÚÀ·”Î50mL0.55mol/LNaOH»Ð“∫Ω¯––∑¥”¶£¨”Î…œ ˆ µ—Èœý±»£¨À˘«Û÷–∫Õ»»___(ÃÓ°∞œýµ»°¢≤ªœýµ»°±)°£
¢Ð»Ù∑¥”¶«∞»Ð“∫“‘º∞÷–∫Õ∫ÛµƒªÏ∫œ“∫µƒ√Ð∂»æ˘…ËŒ™1g/cm3£¨ªÏ∫œ«∞À·”κӵƒŒ¬∂»æ˘Œ™t1£¨ªÏ∫œ∫ۻГ∫µƒŒ¬∂»Œ™t2£¨±»»»»ðŒ™4.18J/(g°§°Ê)£¨‘Ú÷–∫Õ»»¶§H=___°£
£®3£©—ß…˙““”√2mol/Lµƒ¡ÚÀ·¿¥≤‚∂®”Ζø¡£∫Õ–ø∑€∑¥”¶µƒøϬ˝£¨…˺∆»ÁÕº◊∞÷√£∫
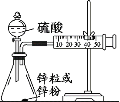
∏√…˙¡Ω¥Œ µ—È≤‚∂® ±º‰æ˘…Ë∂®Œ™10min£¨‘ÚÀ˚ªπ“™≤‚∂®µƒ¡Ì“ª∏ˆ ˝æð «£∫___°£
¢⁄»Ù“™ºı–°≤˙…˙H2µƒÀŸ¬ ∂¯”÷≤ª”∞œÏ≤˙…˙H2µƒ◊Сø£¨”¶œÚ¡ÚÀ·÷–º”»Î___(ÃÓ◊÷ƒ∏)
a.Na2CO3»Ð“∫ b.K2SO4»Ð“∫ c.NaNO3»Ð“∫ d.ÀÆ e.CuSO4»Ð“∫
°æ¥∞∏°øNaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l) °˜H=-57.3kJ/mol Œ¬∂»º∆∫Õª∑–Œ≤£¡ßΩ¡∞Ë∞Ù ¥Û…’±≠…œ√ª”–∏«”≤÷Ω∞ªÚ≈ðƒ≠ÀСœ∞ ∆´¥Û œýµ» °˜H=
Na2SO4(aq)+H2O(l) °˜H=-57.3kJ/mol Œ¬∂»º∆∫Õª∑–Œ≤£¡ßΩ¡∞Ë∞Ù ¥Û…’±≠…œ√ª”–∏«”≤÷Ω∞ªÚ≈ðƒ≠ÀСœ∞ ∆´¥Û œýµ» °˜H=![]() kJ/mol 10minƒ⁄◊¢…‰∆˜ªÓ»˚“∆∂صƒæý¿ÎªÚ10minƒ⁄≤˙…˙«‚∆¯µƒÃª˝ bd
kJ/mol 10minƒ⁄◊¢…‰∆˜ªÓ»˚“∆∂صƒæý¿ÎªÚ10minƒ⁄≤˙…˙«‚∆¯µƒÃª˝ bd
°æΩ‚Œˆ°ø
(1)∏˘æðÀ·ºÓ÷–∫Õ»»µƒ∫¨“ Ȗ¥»»ªØ—ß∑Ω≥Ã Ω£ª
(2)¢Ÿ“¿æð÷–∫Õ»»≤‚∂® µ—ȵƒπ˝≥Ã∫Õ“«∆˜∑÷Œˆ÷–∫Õ»» µ—È ±À˘–˵ƒ≤£¡ß“«∆˜£ª
¢⁄∏˘æðÀ˘∏¯µƒ◊∞÷√Õº£¨ø…÷™»±…Ÿ”≤÷Ω∞£¨¥Û…’±≠…œ»Á≤ª∏«”≤÷Ω∞£¨ª· π“ª≤ø∑÷»»¡ø…¢ ߣª
¢€«øÀ·«øºÓµƒœ°»Ð“∫£¨∑˚∫œ÷–∫Õ»»µƒ≤‚∂®Ãıº˛£ª
¢Ð∏˘æðπ´ Ω÷±Ω”À„≥ˆ£ª
(3)¢Ÿ“™≤‚∂®∑¥”¶ÀŸ¬ £¨‘Úªπ–Ë“™≤‚∂®µƒ¡Ì“ª∏ˆ ˝æ𠒺صΩ∆¯ÃµƒÃª˝;
¢⁄∏˘æð”∞œÏ∑¥”¶ÀŸ¬ “ÚÀÿ∫Õ µ÷ ∑¢…˙µƒ∑¥”¶Ω¯––∑÷Œˆ°£
(1) ÷–∫Õ»» ˝÷µŒ™57.3 kJ/mol£¨∑¥”¶∑≈»»£¨‘Ú÷–∫Õ»»µƒ»»ªØ—ß∑Ω≥Ã Ω£∫NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l) °˜H=-57.3kJ/mol£¨π ¥∞∏Œ™£∫NaOH(aq)+
Na2SO4(aq)+H2O(l) °˜H=-57.3kJ/mol£¨π ¥∞∏Œ™£∫NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l) °˜H=-57.3kJ/mol£ª
Na2SO4(aq)+H2O(l) °˜H=-57.3kJ/mol£ª
(2) ¢Ÿ“¿æð¡ø»»º∆µƒΩ·π˚∫Õ‘≠¿Ì∑÷Œˆ£¨≤‚∂®÷–∫Õ»» µ—È ±À˘–˵ƒ≤£¡ß“«∆˜”–…’±≠°¢¡øÕ≤°¢Œ¬∂»º∆°¢ª∑–Œ≤£¡ßΩ¡∞Ë∞Ù£¨π ¥∞∏Œ™£∫Œ¬∂»º∆°¢ª∑–Œ≤£¡ßΩ¡∞Ë∞Ù£ª
¢⁄ µ—È◊∞÷√±£Œ¬°¢∏Ù»»–ßπ˚±ÿ–Î∫√£¨∑Ò‘Ú”∞œÏ µ—ÈΩ·π˚£¨À˘“‘◊∞÷√»±…Ÿ”≤÷Ω∞ªÚ≈ðƒ≠ÀСœ∞£¨π ¥∞∏Œ™£∫¥Û…’±≠…œ√ª”–∏«”≤÷Ω∞ªÚ≈ðƒ≠ÀСœ∞£ª
¢€«øÀ·«øºÓµƒœ°»Ð“∫£¨∑˚∫œ÷–∫Õ»»µƒ≤‚∂®Ãıº˛£¨À˘«Û÷–∫Õ»»œýµ»£¨π ¥∞∏Œ™£∫œýµ»£ª
¢Ð”…π´ Ω£∫°˜H=![]() =
=![]() kJ/mol£¨π ¥∞∏Œ™£∫°˜H=
kJ/mol£¨π ¥∞∏Œ™£∫°˜H=![]() kJ/mol£ª
kJ/mol£ª
(3)¢Ÿ“™≤‚∂®∑¥”¶ÀŸ¬ £¨‘Úªπ–Ë“™≤‚∂®µƒ¡Ì“ª∏ˆ ˝æ𠒺صΩ∆¯ÃµƒÃª˝£¨π ¥∞∏Œ™£∫10minƒ⁄◊¢…‰∆˜ªÓ»˚“∆∂صƒæý¿ÎªÚ10minƒ⁄≤˙…˙«‚∆¯µƒÃª˝£ª
¢⁄»Áπ˚∑¥”¶π˝”⁄æÁ¡“£¨Œ™¡Àºıª∫∑¥”¶ÀŸ¬ ∂¯”÷≤ªºı…Ÿ≤˙…˙«‚∆¯µƒ¡ø°£a. º”»ÎNa2CO3»Ð“∫£¨—ŒÀ·”ÎúÀ·ƒ∆∑¥”¶£¨«‚∆¯¡øºı…Ÿ£¨¥ÌŒÛ£ªb.º”»ÎK2SO4»Ð“∫£¨—ŒÀ·µƒ≈®∂»ºı–°£¨∑¥”¶ÀŸ¬ ºı–°£¨’˝»∑£ªc.º”»ÎNaNO3»Ð“∫£¨œıÀ·æþ”–«ø—ıªØ–‘£¨≤ªƒÐ∑≈≥ˆ«‚∆¯£¨¥ÌŒÛ£ªd. º”»Î’Ù¡ÛÀÆ£¨—ŒÀ·µƒ≈®∂»ºı–°£¨∑¥”¶ÀŸ¬ ºı–°£¨’˝»∑£ªe. º”»ÎCuSO4»Ð“∫£¨–ø”ÎÕ≠¿Î◊”∑¥”¶÷√ªª≥ˆÕ≠£¨«‚∆¯¡øºı…Ÿ£¨¥ÌŒÛ£ªπ ¥∞∏Œ™£∫bd°£


 ø⁄À„Âø®º””¶”√ºؗµœµ¡–¥∞∏
ø⁄À„Âø®º””¶”√ºؗµœµ¡–¥∞∏ ◊€∫œ◊‘≤‚œµ¡–¥∞∏
◊€∫œ◊‘≤‚œµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø≥£Œ¬œ¬£¨œ¬¡–»Ð“∫÷–∏˜◊È¿Î◊”“ª∂®ƒÐ¥Û¡øπ≤¥Êµƒ «
A. π Ø»Ô ‘“∫≥ ∫Ï…´µƒ»Ð“∫÷–£∫Na£´°¢Al3£´°¢NO3£≠°¢![]()
B.![]() £Ω0.1 mol°§L£≠1µƒ»Ð“∫£∫Na£´°¢K£´°¢CO32£≠°¢NO3£≠
£Ω0.1 mol°§L£≠1µƒ»Ð“∫£∫Na£´°¢K£´°¢CO32£≠°¢NO3£≠
C.∫¨”–0.1 mol°§L£≠1 HCO3£≠µƒ»Ð“∫£∫Na£´°¢Fe3£´°¢NO3£≠°¢SCN£≠
D.”…ÀƵÁ¿Î≤˙…˙µƒc(H£´)£Ω10£≠12 mol°§L£≠1µƒ»Ð“∫£∫NH4£´£¨SO42£≠°¢HCO3£≠°¢Cl£≠
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø√ª ≥◊”À·±˚ı•ºÚ≥∆PG£¨ «“ª÷÷∞◊…´∑€ƒ©£¨ƒ—»Ð”⁄ÀÆ£¨Œ¢»Ð”⁄√Þ◊””Õµ»”Õ÷¨£¨ «≥£”√µƒ ≥”√”Õøπ—ıªØº¡°£∆‰Ω·ππºÚ Ω»ÁÕºÀ˘ æ°£
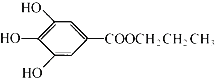
“—÷™£∫PGæ≠ÀÆΩ‚ø…◊™ªØŒ™√ª ≥◊”À·£¨√ª ≥◊”À·ƒÐ”ÎNaHCO3»Ð“∫∑¥”¶…˙≥…CO2
ªÿ¥œ¬¡–Œ £∫
(1)¥”∑÷◊”Ω·ππªÚ–‘÷ …œø¥£¨PGæþ”–øπ—ıªØ◊˜”√µƒ÷˜“™‘≠“Ú «£∫______£®Œƒ◊÷ºÚ ˆ£©
(2)1mol√ª ≥◊”À·◊Ó∂ýø…“‘”Î∫¨________molúÀ·ƒ∆µƒ»Ð“∫∑¢…˙∑¥”¶°£
(3)–¥≥ˆPG‘⁄NaOH»Ð“∫÷–ÀÆΩ‚µƒªØ—ß∑Ω≥Ã Ω£∫_______________________°£
(4)√ª ≥◊”À·”–∂ý÷÷Õ¨∑÷“Ïππ㨖¥≥ˆ∆‰÷–∑˚∫œœ¬¡–“™«ÛµƒÕ¨∑÷“ÏππõƒΩ·ππºÚ Ω£∫____°£
a£Æ∫¨”–±Ωª∑£¨«“±Ωª∑…œµƒ“ª‰Â¥˙ŒÔ÷ª”–“ª÷÷£ª
b£Æº»ƒÐ∑¢…˙“¯æµ∑¥”¶£¨”÷ƒÐ∑¢…˙ÀÆΩ‚∑¥”¶°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø“—÷™œ¬¡–»»ªØ—ß∑Ω≥Ã Ω£∫Zn(s) +![]() O2(g) £ΩZnO(s) ¶§H1£Ω£≠351.1kJ/mol
O2(g) £ΩZnO(s) ¶§H1£Ω£≠351.1kJ/mol
Hg(l) +![]() O2(g) £Ω HgO(s) ¶§H2£Ω£≠90.7kJ/mol
O2(g) £Ω HgO(s) ¶§H2£Ω£≠90.7kJ/mol
”…¥Àø…÷™Zn(s) + HgO(s) £Ω ZnO(s) + Hg(l)µƒ¶§H3£¨∆‰÷–¶§H3µƒ÷µ «
A.£≠260.4 kJ/molB.£≠254.6 kJ/molC.£≠438.9 kJ/molD.£≠441.8 kJ/mol
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø2SO2(g)£´O2(g))![]() 2SO3(g)∑¥”¶π˝≥õƒƒÐ¡ø±‰ªØ»ÁÕºÀ˘ 棨“—÷™1molSO2(g)±ª—ıªØŒ™1molSO3(g)µƒ¶§H=£≠akJ/mol(a©É0)°£ªÿ¥œ¬¡–Œ £∫
2SO3(g)∑¥”¶π˝≥õƒƒÐ¡ø±‰ªØ»ÁÕºÀ˘ 棨“—÷™1molSO2(g)±ª—ıªØŒ™1molSO3(g)µƒ¶§H=£≠akJ/mol(a©É0)°£ªÿ¥œ¬¡–Œ £∫
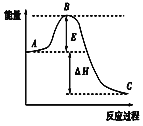
£®1£©Õº÷–A±Ì æ£∫__£¨Eµƒ¥Û–°∂‘∏√∑¥”¶µƒ∑¥”¶»»¶§H__(ÃÓ°∞ «°±ªÚ°∞∑Ò°±)”–”∞œÏ°£∏√∑¥”¶Õ®≥£”√V2O5◊˜¥þªØº¡£¨º”V2O5ª· πÕº÷–Bµ„__(ÃÓ°∞…˝∏þ°±ªÚ°∞ΩµµÕ°±)£¨¿Ì”… «__°£
£®2£©Õº÷–¶§H=__kJ/mol°£
£®3£©‘⁄“ª∂®Œ¬∂»œ¬£¨Ω´2molSO2∫Õ1molO2∑≈‘⁄“ª√б’»ð∆˜÷–£¨‘⁄¥þªØº¡◊˜”√œ¬≥‰∑÷∑¥”¶°£≤‚µ√∑¥”¶∑≈≥ˆµƒ»»¡ø__(ÃÓ°∞µ»”⁄°±°¢°∞¥Û”⁄°±ªÚ°∞–°”⁄°±)2akJ°£
£®4£©V2O5µƒ¥þªØ—≠ª∑ª˙¿Ìø…ƒÐŒ™£∫V2O5—ıªØSO2 ±£¨◊‘º∫±ªªπ‘≠Œ™Àƒº€∑∞ªØ∫œŒÔ£ªÀƒº€∑∞ªØ∫œŒÔ‘Ÿ±ª—ı∆¯—ıªØ°£–¥≥ˆ∏√¥þªØ—≠ª∑ª˙¿ÌµƒªØ—ß∑Ω≥Ã Ω£∫
¢Ÿ__£ª¢⁄4VO2£´O2=2V2O5
£®5£©“—÷™πÃ赕÷ ¡Úµƒ»º…’»»Œ™bkJ/mol£¨º∆À„”…S(s)…˙≥…3molSO3(g)µƒ¶§H=___°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø”√ÕºÀ˘ æ◊∞÷√ºÏ—È““œ© ±≤ª–Ë“™≥˝‘”µƒ «
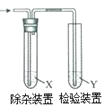
““œ©µƒ÷∆±∏ | ‘º¡X | ‘º¡Y | |
A | CH3CH2Br”ÎNaOH““¥º»Ð“∫π≤»» | H2O | KMnO4À·–‘»Ð“∫ |
B | CH3CH2Br”ÎNaOH““¥º»Ð“∫π≤»» | H2O | Br2µƒCCl4»Ð“∫ |
C | CH3CH2OH”Î≈®H2SO4π≤»»÷¡170°Ê | NaOH»Ð“∫ | KMnO4À·–‘»Ð“∫ |
D | CH3CH2OH”Î≈®H2SO4π≤»»÷¡170°Ê | NaOH»Ð“∫ | Br2µƒCCl4»Ð“∫ |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø≥£”√“©©ÅÙ«±ΩÀÆ—Ó∞∑£¨∆‰∫œ≥…¬∑œþ»ÁÕº°£ªÿ¥œ¬¡–Œ £∫
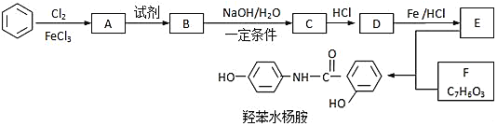
“—÷™£∫![]()
£®1£©Ù«±ΩÀÆ—Ó∞∑µƒªØ—ß ΩŒ™___°£1molÙ«±ΩÀÆ—Ó∞∑◊Ó∂ýø…“‘∫Õ___molNaOH∑¥”¶°£
£®2£©D÷–πŸƒÐÕ≈µƒ√˚≥∆___°£
£®3£©A°˙B∑¥”¶À˘º”µƒ ‘º¡ «___°£
£®4£©F¥Ê‘⁄∂ý÷÷Õ¨∑÷“Ïππð£
FµƒÕ¨∑÷“ÏππÃÂ÷–º»ƒÐ”ÎFeCl3∑¢…˙œ‘…´∑¥”¶£¨”÷ƒÐ∑¢…˙“¯æµ∑¥”¶£¨«“∫À¥≈π≤’Ò«‚∆◊œ‘ æ4◊È∑£¨∑Â√ʪ˝÷Ʊ»Œ™1£∫2£∫2£∫1µƒÕ¨∑÷“ÏππõƒΩ·ππºÚ Ω___°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø≤‚∂®»Ð“∫µÁµº¬ µƒ±‰ªØ «∂®¡ø—–æøµÁΩ‚÷ ‘⁄»Ð“∫÷–∑¥”¶πʬ…µƒ“ª÷÷∑Ω∑®£¨»Ð“∫µÁµº¬ ‘Ω¥Û∆‰µºµÁƒÐ¡¶‘Ω«ø°£ “Œ¬œ¬£¨”√0.100molL-1µƒNH3H2OµŒ∂®10.00mL≈®∂»æ˘Œ™0.100molL-1HCl∫ÕCH3COOHµƒªÏ∫œ»Ð“∫£¨À˘µ√µÁµº¬ «˙œþ»ÁÕºÀ˘ æ°£œ¬¡–Àµ∑®’˝»∑µƒ «£® £©
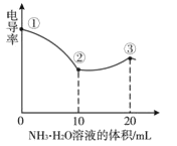
A.¢Ÿµ„»Ð“∫£∫pH◊Ó¥Û
B.»Ð“∫Œ¬∂»£∫¢Ÿ∏þ”⁄¢⁄
C.¢€µ„»Ð“∫÷–£∫c(Cl-)£æc(CH3COO-)
D.¢⁄µ„»Ð“∫÷–£∫c(NH4+)+c(NH3H2O)£æc(CH3COOH)+c(CH3COO-)
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ°∞±ÀÆ÷–¥Ê‘⁄◊≈œ¬¡–∆Ω∫‚£∫NH3°§H2O![]() NH4+£´OH£≠£¨»Ù“™ π∆Ω∫‚œÚƒÊ∑¥”¶∑ΩœÚ“∆∂Ø£¨Õ¨ ± πc(OH£≠)‘ˆ¥Û£¨”¶º”»ÎµƒŒÔ÷ ªÚ≤…»°µƒ¥Î © «£® £©
NH4+£´OH£≠£¨»Ù“™ π∆Ω∫‚œÚƒÊ∑¥”¶∑ΩœÚ“∆∂Ø£¨Õ¨ ± πc(OH£≠)‘ˆ¥Û£¨”¶º”»ÎµƒŒÔ÷ ªÚ≤…»°µƒ¥Î © «£® £©
¢ŸNH4ClπÃ㪢⁄¡ÚÀ·£ª¢€NaOHπÃ㪢ÐÀÆ£ª¢ðº”»»£ª¢Þº”»Î…Ÿ¡øMgCl2πÃð£
A.¢Ÿ¢⁄¢€¢ðB.¢€¢ÞC.¢€D.¢€¢ð
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
∞Ÿ∂»÷¬–≈ - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com