
 ����þ��Ŀǰ�����������졢���ա���е���졢���µȲ�ҵ�е���Ѹ�ͷ�չ��
����þ��Ŀǰ�����������졢���ա���е���졢���µȲ�ҵ�е���Ѹ�ͷ�չ������ ��1���������Ͻ���ϣ��������Ͻ�þ���Ͻ�ȣ�Ӳ�ȴ������۷�����
��2����þ������þ�Ļ�����ǿ���������Կ�ʼþ������������������
��Mg���Al���ã���Mg������NaOH��Һ��Ӧ����Al����NaOH��Һ��Ӧ����Al��������ʧ��������Al3+��Al3+���OH-����AlO2��þ�������������������õ����ӱ���ԭ������������ʴ��
��� �⣺��1����Ϊ���Ͻ���ϣ��������Ͻ�þ���Ͻ�ȣ�Ӳ�ȴ������ۣ��������Ͻ�����ڵ����ϴ����л��ϳɲ��ϣ�
��ѡ��BC��
��2����þ������þ�Ļ�����ǿ���������Կ�ʼþ������������������ԭ���װ��ͼ��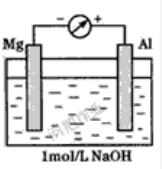 ��
��
�ʴ�Ϊ�� ��
��
��Mg���Al���ã���Mg������NaOH��Һ��Ӧ����Al����NaOH��Һ��Ӧ����Al��������ʧ��������Al3+��Al3+���OH-����AlO2���缫��ӦʽΪ��Al+4OH--3e-=AlO2-+2H2O��þ�������������������õ����ӱ���ԭ���缫��ӦʽΪ��O2+2H2O+4e-=4OH-��
�ʴ�Ϊ��Al+4OH--3e-=AlO2-+2H2O��O2+2H2O+4e-=4OH-��
���� ���⿼����Ԫ�ػ���������ʣ����ؿ���þ�������ʣ���Ϥ�Ͻ�ĸ�����ʣ���ȷԭ��ع��������ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4 | B�� | 5 | C�� | 6 | D�� | 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��Ӧ���ʱ�С���㣬�÷�Ӧһ�����Է����� | |
| B�� | ��ʪ���PH��ֽ��ϡ������Һ��pHΪ3.52 | |
| C�� | ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�� | |
| D�� | ��ľ�ң�K2CO3���Ǽطʣ�������ǵ��ʣ������ʩ�ÿ�����߷�Ч |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͭ��Һ�м��������NaHS��Һ��Cu2++2HS-�TCuS��+H2S�� | |
| B�� | NH4Al��SO4��2��Һ��������Ba��OH��2��Һ��ϣ�NH4++Al3++2SO42-+2Ba2++4OH-�T2BaSO4��+Al��OH��3��+NH3•H2O | |
| C�� | ��Na2S2O3��Һ��ͨ������������S2O32-+2Cl2+3H2O�T2SO32-+4Cl-+6H+ | |
| D�� | Ǧ�����س��ʱ��������Ӧ��PbSO4+2H2O-2e-�TPbO2+4H++SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
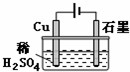
| A�� | �������У�ͭ�缫����H2���� | |
| B�� | �����ڣ�����Ӧ����ʽΪCu+H2SO4$\frac{\underline{\;ͨ��\;}}{\;}$CuSO4+H2�� | |
| C�� | ���һ��ʱ���ʯī�缫����ͭ���� | |
| D�� | �����������У�H+��Ũ�ȼ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4 | B�� | Na2O2 | C�� | Fe��OH��3 | D�� | AlCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ƕ�����ˮ��Ӧ���ɶ�Ӧ���� | |
| B�� | ��״�������Ƕ�����ɫ��ζ������ | |
| C�� | ��������Ԫ�ص�����������NO��NO2��SO2 | |
| D�� | ʵ���ҿ�������������ԭ��Ӧ�ֱ��Ʊ�NO��NO2��SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.24L | B�� | 3.92L | C�� | 3.36L | D�� | 2.8L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��һ���¶��£���1L����̶����ܱ������м���1molA��g����������Ӧ2A��g��?B��g��+C��g����B�����ʵ�����ʱ��ı仯��ͼ��ʾ�� 0-2min�ڵ�ƽ����Ӧ����v��A��=0.1mol/��L•min������ͬ�¶��£�����ʼ����A��g�������ʵ�����ԭ����2������ƽ��ʱbe��ԭ����2����
��һ���¶��£���1L����̶����ܱ������м���1molA��g����������Ӧ2A��g��?B��g��+C��g����B�����ʵ�����ʱ��ı仯��ͼ��ʾ�� 0-2min�ڵ�ƽ����Ӧ����v��A��=0.1mol/��L•min������ͬ�¶��£�����ʼ����A��g�������ʵ�����ԭ����2������ƽ��ʱbe��ԭ����2�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com