
分析 查表得:K(NH3)=1.75×10-5,对K(NH3) 取负对数,即得pK(NH3)[如同 pH=-lgc(H+)]
pK(NH3)=-lgK(NH3)=4.76
pOH=pK(NH3)-lg ($\frac{n(N{H}_{3})}{n(N{H}_{4}Cl)}$)
lg($\frac{n(N{H}_{3})}{n(N{H}_{4}Cl)}$)=pK(NH3)-(14-pH)=4.76-4.0=0.76
$\frac{n(N{H}_{3})}{n(N{H}_{4}Cl)}$=5.75
n(NH4Cl)=$\frac{n(N{H}_{3})}{5.75}$=$\frac{1.5mol/L×0.0035L}{5.75}$=0.00091mol,依据物质的量和摩尔质量计算所需氯化铵的质量.
解答 解:查表得:K(NH3)=1.75×10-5,
对K(NH3) 取负对数,即得pK(NH3)[如同 pH=-lgc(H+)]
pK(NH3)=-lgK(NH3)=4.76
pOH=pK(NH3)-lg ($\frac{n(N{H}_{3})}{n(N{H}_{4}Cl)}$)
lg($\frac{n(N{H}_{3})}{n(N{H}_{4}Cl)}$)=pK(NH3)-(14-pH)=4.76-4.0=0.76
$\frac{n(N{H}_{3})}{n(N{H}_{4}Cl)}$=5.75
n(NH4Cl)=$\frac{n(N{H}_{3})}{5.75}$=$\frac{15mol/L×0.0035L}{5.75}$=0.0091mol
m(NH4Cl)=n(NH4Cl)×M(NH4Cl)=0.0091mol×53.5g/mol=0.488g,
答:若配制pH=10.00的NH3-NH4Cl缓冲溶液1L,已知用去15mol•L-1氨水3.5ml,需加入NH4Cl质量为0.488g.
点评 本题考查了缓冲溶液的形成和配制,主要是配制溶液需要的溶质量的计算,题目难度较大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,2.24LSO2与O2混合气体中所含氧原子数为0.2NA | |
| B. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 标准状况下,20gD20分子中所含中子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
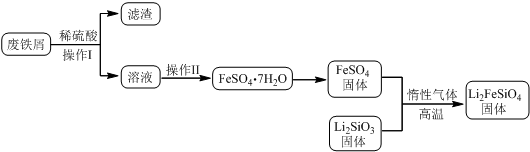
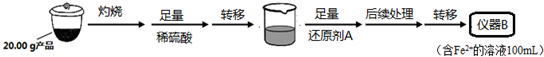
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积 | 20.00mL | 19.98mL | 21.38mL | 20.02mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 充电时阳极反应可表示为LiFePO4-xe-=Li1-xFePO4+xLi+ | |
| B. | 充电时阴极反应可表示为xLi++xe-+6C=LixC6 | |
| C. | 放电时负极反应可表示为LixC6-xe-=xLi++6C | |
| D. | 放电时Li+从左向右通过离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 250mL | B. | 375mL | C. | 475mL | D. | 500mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c[NH3•H2O] | B. | c[H+] | C. | c[OH-] | D. | c[NH4+] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com