
A、 |
B、 |
C、 |
D、 |


科目:高中化学 来源: 题型:
| A、35Cl的质量数为35,所以氯元素的相对原子质量为35 |
| B、35Cl和37Cl为不同的核素,有不同的化学性质 |
| C、实验室制备氯气可以用排饱和食盐水的方法集气收集 |
| D、1.12LCl2含有1.7NA个质子(NA表示阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离产生的c(H+)=1.0×10-2 mol?L-1 |
| B、pH=12 |
| C、pH=2 |
| D、混合后的溶液溶质的物质的量浓度为0.02 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在豆浆里加入盐卤做豆腐 |
| B、三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
| C、一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路 |
| D、在河流入海处易形成沙洲 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐--③④ |
| B、纯净物--④⑤⑥ |
| C、碱--④⑤ |
| D、混合物--②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
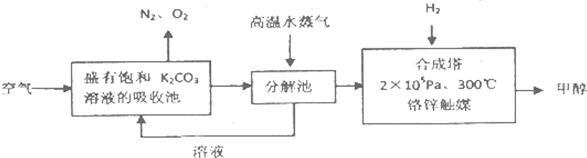

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com