
| A. | 需要加热才能发生的反应是吸热反应 | |
| B. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出热量少 | |
| C. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 | |
| D. | 由热化学方程式 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
分析 A、某些放热反应也需要加热才能发生;
B、等质量的硫蒸汽和硫固体,前者的能量高;
C、化学反应的反应热取决于反应物和生成物的能量的差值;
D、合成氨的反应为可逆反应,不能进行彻底.
解答 解:A、某些放热反应也需要加热才能发生,故需要加热才能发生的反应不一定是吸热反应,也可能是放热反应,故A错误;
B、等质量的硫蒸汽和硫固体,前者的能量高,故当完全燃烧生成二氧化硫时,放出的热量前者多,故B错误;
C、化学反应的反应热取决于反应物和生成物的能量的差值,即取决于始态和终态,与反应路径无关,故C正确;
D、合成氨的反应为可逆反应,不能进行彻底,故1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,释放出的热量小于92kJ,故D错误.
故选C.
点评 本题考查热化学方程式的含义和反应热的大小判断,题目难度不大,做题时要注意热化学方程式中反应热与物质的物质的量成正比,取决于始态和终态,与反应路径无关.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率通常用单位时间内反应物或生成物的质量变化来表示 | |
| B. | 化学反应速率的单位由浓度单位决定 | |
| C. | 在反应过程中,反应物的浓度逐渐变小,所以用反应物表示的化学反应速率为负值 | |
| D. | 用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 离子化合物一定可以导电 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
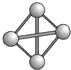 W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.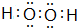 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: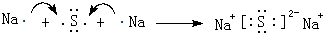 .
.| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01 mol•L-1 | B. | 0.017 mol•L-1 | C. | 0.05 mol•L-1 | D. | 0.50 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com