
 ������и��⣺
������и��⣺

 ̽���빮�̺��Ͽ�ѧ����������ϵ�д�
̽���빮�̺��Ͽ�ѧ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ܷ�Ӧ�����ӷ���ʽΪ��Mg+H2O2+2H+=Mg2++2H2O |
| B�������ĵ缫��ӦΪ��H2O2+2H++2e-=2H2O |
| C������ʱ��������Χ��ˮ��pH���� |
| D����ع���ʱ����Һ�е�H+���ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ǿ����Һ������H2�� |
| B��������Һ������H2�� |
| C�����߲�����H2һ���� |
| D�����Ƚ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
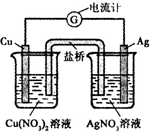
| A����⾫��ͭʱ�ǽ�����ת��Ϊ��ѧ�ܣ���·��ÿͨ��2mole-ʱ�������ͻ��ܽ�64��ͭ |
| B����⾫��ͭʱ����Ϊ��ͭ������Ϊ��ͭ���������е���ʲ���Ҫ���� |
| C�������������϶����������Ϊ��������������������������������Ϊ���� |
| D����ƹ����е��Һ��Ҫ���ϸ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4��C2H4 |
| B��C2H6��C3H6 |
| C��C2H4��C2H6 |
| D��C2H2��C2H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�1L 0.1mol/L��NH4NO3��Һ�е�ԭ����Ϊ0.2NA |
| B�����³�ѹ�£�22.4L CH4����4NA��C-H���ۼ� |
| C��2mol N2��2mol H2��ϳ�ַ�Ӧ��ת�Ƶĵ�����ĿΪ4NA |
| D��10L pH=1��������Һ�к��е�H+������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ϡ���ᣬ��Һ��ƣ�Fe+4H++NO3-=Fe3++NO��+2H2O |
| B��Na2CO3��Һ��ʹ��̪��Һ��죺CO32-+H2O?HCO3-+OH- |
| C��0.1mol/LCH3COOH��Һ��pH��1��CH3COOH?CH3COO-+H+ |
| D����NaHCO3��Һ�м�������Ca��OH��2��Һ���ְ�ɫ������HCO3-+Ca2++OH-=CaCO3��+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com