
室温下,在0.2mol/L Al2(SO4)3溶液中,逐滴加入1.0mol/L NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:
Al3+ + 3OH-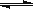 Al(OH)3
Al(OH)3
B.a-b段,溶液pH增大,Al3+浓度不变
C.b-c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
【知识点】镁、铝的重要化合物 C2 H3
【答案解析】C 解析: A.硫酸铝为强酸弱碱盐,水解显酸性,水解离子反应为Al3++3H2O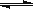 Al(OH)3+3H+,故A错误; B.a-b段,发生H++OH-═H2O,但加入NaOH溶液,总体积增大,则Al3+浓度减小,故B错误; C.b-c段,pH变化不大,主要发生Al3++3OH-═Al(OH)3↓,则加入的OH-主要用于生成Al(OH)3沉淀,故C正确; D.c点后pH发生突变,NaOH过量,Al(OH)3沉淀开始溶解,生成NaAlO2,碱性较强,而d点pH>10,NaOH远远过量,故D错误。
Al(OH)3+3H+,故A错误; B.a-b段,发生H++OH-═H2O,但加入NaOH溶液,总体积增大,则Al3+浓度减小,故B错误; C.b-c段,pH变化不大,主要发生Al3++3OH-═Al(OH)3↓,则加入的OH-主要用于生成Al(OH)3沉淀,故C正确; D.c点后pH发生突变,NaOH过量,Al(OH)3沉淀开始溶解,生成NaAlO2,碱性较强,而d点pH>10,NaOH远远过量,故D错误。
【思路点拨】本题考查了盐类水解及复分解反应,注意氢氧化铝的两性及图中c点pH突变为解答的关键,明确b→c段中铝离子过量,题目难度不大.


科目:高中化学 来源: 题型:
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
A.①③ B.①④ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.25 ℃时,在pH=2的1.0 L H2SO4溶液中含有H+数目为0.02NA
B.1 mol Na2O2固体中含离子总数与1 mol CH4中所含共价键数目相等
C.将含有1 mol FeCl3溶质的饱和溶液加入沸水中可以得到NA个Fe(OH)3胶粒
D.向含有FeI2的溶液中通入适量氯气,当有1 mol Fe2+被氧化时,该反应转移电子的数目至少为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00 mL 0.049 mol·L-1的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65 mL 0.020 mol·L-1的酸性KMnO4溶液完全作用,则在上述反应中,羟胺的氧化产物是[已知:FeSO4+KMnO4+H2SO4—→Fe2(SO4)3+K2SO4+MnSO4+H2O(未配平)]( )
A.N2 B.N2O C.NO D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的
4种钠盐溶液pH如下表:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法中, 正确的是( )
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生活、社会可持续发展密切相关。下列说法不正确的是
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.催化转化机动车尾气为无害气体,能消除酸雨 和雾霾的发生
和雾霾的发生
C.研发高效低毒的农药,降低 蔬菜的农药残留量
蔬菜的农药残留量
D.积极开发废电池的综合利用技术,防止电池中的重金属等污染土壤和水体
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,17g甲基(-14CH3)所含的中子数为9NA
B.标准状况下, 11.2L苯中含有的碳碳双键数为1.5NA
11.2L苯中含有的碳碳双键数为1.5NA
C.42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA
D.5.6g铁与0.1mol氯 气在点燃条件下充分反应,转移的电子数为0.3NA
气在点燃条件下充分反应,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
配平下列方程式
(1)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
 Ce3++
Ce3++ H2O2+
H2O2+ H2O===
H2O=== Ce(OH)4↓+
Ce(OH)4↓+ ________
________
(2)完成“氧化除铁”步骤中反应的离子方程式:
 Fe(OH)2+
Fe(OH)2+ ClO-+
ClO-+ ________===
________=== Fe(OH)3+
Fe(OH)3+ Cl-
Cl-
(3)配平反应的离子方程式:
 Mn2++
Mn2++ ClO
ClO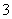 +
+ H2O===
H2O=== MnO2↓+
MnO2↓+ Cl2↑+
Cl2↑+ ________。
________。
(4)配平用钙线脱氧脱磷的化学方程式:
 P+
P+ FeO+
FeO+ CaO
CaO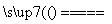
 Ca3(PO4)2+
Ca3(PO4)2+ Fe
Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
标出电子转移的方向和数目。
2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2 5NH4NO3 = 4N2↑+ 9H2O + 2HNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com