
| A. | lH、2H、3H为同素异形体 | B. | lH、2H、3H互为同位素 | ||
| C. | lH、2H、3H的质量数相同 | D. | lH、2H、3H为同分异构体 |
分析 有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;
具有相同分子式而结构不同的化合物互为同分异构体;
相同元素组成,不同形态的单质互为同素异形体.
解答 解:A.1H、2H、3H质子数相同,中子数不同,互为同位素,同素异形体是同种元素的不同种单质,故A错误;
B.1H、2H、3H质子数相同,中子数不同,互为同位素,故B正确;
C.1H、2H、3H质子数相同,中子数不同,质量数不同,故C错误;
D.1H、2H、3H质子数相同,中子数不同,互为同位素,分子式相同,结构不同的互称为同分异构体,故D错误,
故选B.
点评 本题考查同位素的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:解答题
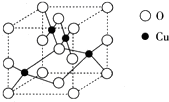 第Ⅵ族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,含第Ⅵ族元素的化合物在研究和生产中有许多重要用途,请回答下列问题.
第Ⅵ族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,含第Ⅵ族元素的化合物在研究和生产中有许多重要用途,请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
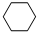 (g)$\stackrel{催化剂}{?}$
(g)$\stackrel{催化剂}{?}$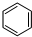 (g)+3H2(g)△H
(g)+3H2(g)△H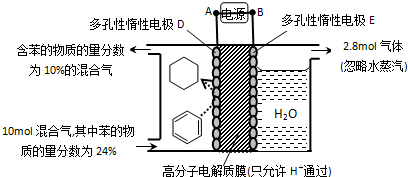
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋清溶液中加入醋酸铅溶液,会发生盐析 | |
| B. | 青苹果中富含苹果酸,因此苹果是酸性食物 | |
| C. | 过氧化钠可用于呼吸面具或潜水艇中作为氧气的来源 | |
| D. | 氢氧化钠、碳酸钙、氢氧化铝等可作为抗酸药 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含碳元素的化合物都是有机物 | B. | 乙烯的结构简式是C2H4 | ||
| C. | 乙酸的酸性比碳酸弱 | D. | 蔗糖的分子式是C12H22O11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图①装置可验证酸性:H2CO3>H2SiO3 | |
| B. | 图②装置可用于收集气体H2 CO2 Cl2 NH3 | |
| C. | 图③装置可用于分离CCl4萃取碘水后的有机层和水层 | |
| D. | 图④装置中接通开关后,Zn片腐蚀速率增大,Cu片有气体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 一定有甲烷 | B. | 一定有乙烷 | ||
| C. | 可能是甲烷和乙烷的混合物 | D. | 可能是乙烷和丙烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
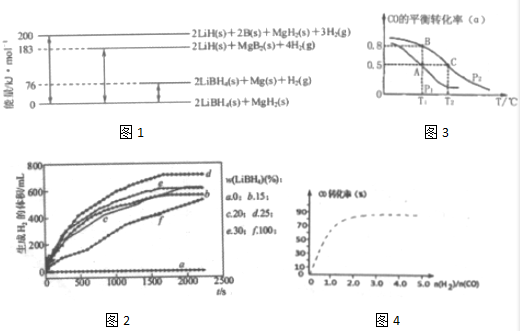
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com