
| A. | 检验溶液中是否含有 CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 | |
| B. | 检验溶液中是否含有 NH4+:先滴加浓 NaOH 溶液并加热,再用湿润的红色石 蕊试纸 | |
| C. | 检验溶液中是否含有 Fe2+:先滴加氯水,再滴加 KSCN 溶液 | |
| D. | 检验溶液中是否含有 SO42-:先滴加氯化钡溶液,再滴加稀盐酸 |
分析 A.能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,原溶液中可能含有亚硫酸根离子、亚硫酸氢根离子;
B.检验铵根离子先用浓碱液加热,然后用湿润的红色石 蕊试纸;
C.检验亚铁离子时,应该先加入硫氰化钾溶液,溶液不变红,然后再加入氯水;
D.加入氯化钡溶液,生成的沉淀可能为氯化银,应该先加入稀盐酸,排除干扰离子.
解答 解:A.滴加稀盐酸,将产生的气体通入澄清石灰水,若石灰水变浑浊,原溶液中不一定含有CO32-,可能含有SO32-、HCO3-等离子,故A错误;
B.检验溶液中是否含有 NH4+的方法为:先滴加浓 NaOH 溶液并加热,再用湿润的红色石蕊试纸,若试纸变蓝,说明原溶液中含有铵根离子,故B正确;
C.检验溶液中是否含有 Fe2+,应该先滴KSCN溶液,溶液不变红,再滴加氯水,顺序不能颠倒,故C错误;
D.检验溶液中是否含有 SO42-,应该先滴加稀盐酸,没有沉淀生成,然后再滴加氯化钡溶液,加入顺序不能颠倒,故D错误;
故选B.
点评 本题考查了化学实验方案的评价,题目难度不大,明确常见离子的性质为解答关键,注意熟练掌握常见离子的检验方法,试题培养了学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:选择题
| A. | 2AB(g)?A2(g)+B2(g)△H>0 | B. | A2(g)+3B2(g)?2AB3(g)△H<0 | ||
| C. | A(s)+B(g)?C(g)+D(g)△H>0 | D. | 2A(g)+B(g)?3C(g)+D(s)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
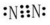 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 | 碳酸氢钠药片 |  |  |
| 如图为铝热反应的实验装置,工业上利用铝热反应大量冶炼金属铁 | 如图现象为丁达尔效应,丁达尔效应可用于鉴别溶液和胶体 | 如图药品属抗酸药,可治疗胃酸过多 | 看到有该标志的丢弃物,应远离并报警 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ③④⑦ | C. | ②⑤⑦ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径/10-10 nm | 0.73 | 1.30 | 1.34 | 1.06 | 0.99 | 1.54 | 0.75 | 1.02 |
| 最高或最低化合价 | -2 | +2 | +1 | +5 | +7 | +1 | -3 | +6 |
| A. | ③和⑤处于同一周期 | |
| B. | 气态氢化物的稳定性④大于⑧ | |
| C. | 上述八种元素最高价氧化物对应的水化物中,⑤的酸性最强 | |
| D. | ①与⑥只能形成一种化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com