
分析 根据c(H+)•c(OH-)=Kw计算某温度下水的离子积常数,温度不变,水的离子积常数不变,根据c(OH-)=$\frac{{K}_{W}}{C({H}^{+})}$计算;纯水溶液中氢离子浓度始终等于氢氧根离子浓度.
解答 解:某温度下,纯水中的c(H+)=2.0×10-7mol•L-1,H2O?OH-+H+,则c(OH-)=c(H+)=2.0×10-7mol•L-1,Kw=c(OH-)×c(H+)=4.0×10-14(mol•L-1)2,若温度不变,滴入稀盐酸,使c(H+)=5×10-4mol/L,则溶液中c(OH-)=$\frac{{K}_{W}}{C({H}^{+})}$=$\frac{4×1{0}^{-14}}{5×1{0}^{-4}}$=8×10-11mol/Lmol/L,此时溶液中的氢氧根全部来源于水的电离,由水电离出的氢离子浓度等于由水电离出的氢氧根离子的浓度,即8×10-11mol/L,
故答案为:8×10-11;8×10-11.
点评 本题考查了水的离子积常数的分析应用,明确氢离子浓度、氢氧根离子浓度和离子积常数之间的关系是解本题关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol乙烷含C-H键的数目为7NA | |
| B. | 1L0.5mol/LNa2S溶液中HS-的数目为0.5NA | |
| C. | 标准状况下,Na与水反应产生22.4 LH2时转移电子数目为2 NA | |
| D. | 含1mol HCOOH的水溶液中含氧原子的总数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 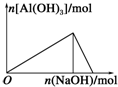 向AlCl3溶液中滴加NaOH溶液 | B. | 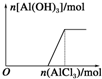 向NaOH溶液中滴加AlCl3溶液 | ||
| C. | 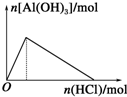 向Na[Al(OH)4]溶液中通入CO2 | D. |  向AlCl3溶液中滴氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | ①②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫有毒,严禁将其添加到任何食品和饮料中 | |
| B. | 饮食“镉大米”会影响骨骼和肾脏,镉元素属于重金属元素 | |
| C. | 使用增塑剂--邻苯二甲酸酯可使聚氯乙烯由弹性塑胶变为硬塑胶 | |
| D. | 面粉生产中禁止添加的过氧化钙(CaO2)中阴阳离子的个数比为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com