

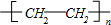 ,G与HBr发生加成反应生成H为CH3CH2Br,由转化关系可知,H在氢氧化钠水溶液、加热条件条件下发生取代反应生成I为CH3CH2OH,I在浓硫酸、加热条件下发生消去反应生成乙烯.D与HCl发生加成反应生成E为CH2=CHCl,E发生加聚反应生成F为
,G与HBr发生加成反应生成H为CH3CH2Br,由转化关系可知,H在氢氧化钠水溶液、加热条件条件下发生取代反应生成I为CH3CH2OH,I在浓硫酸、加热条件下发生消去反应生成乙烯.D与HCl发生加成反应生成E为CH2=CHCl,E发生加聚反应生成F为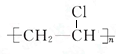 ,据此解答.
,据此解答.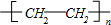 ,G与HBr发生加成反应生成H为CH3CH2Br,由转化关系可知,H在氢氧化钠水溶液、加热条件条件下发生取代反应生成I为CH3CH2OH,I在浓硫酸、加热条件下发生消去反应生成乙烯.D与HCl发生加成反应生成E为CH2=CHCl,E发生加聚反应生成F为
,G与HBr发生加成反应生成H为CH3CH2Br,由转化关系可知,H在氢氧化钠水溶液、加热条件条件下发生取代反应生成I为CH3CH2OH,I在浓硫酸、加热条件下发生消去反应生成乙烯.D与HCl发生加成反应生成E为CH2=CHCl,E发生加聚反应生成F为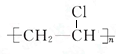 ,
,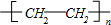 ,故答案为:CH4;CH3CH2Br;
,故答案为:CH4;CH3CH2Br;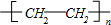 ;
;| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |


科目:高中化学 来源: 题型:
| A、氧化铁和稀硫酸反应:Fe2O3+6H+=2Fe2++3H2O |
| B、碳酸氢钠溶液中加稀硫酸:CO32-+2H+=H2O+CO2↑ |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、Cu(OH)2加入H2SO4:2H++Cu(OH)2=Cu2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
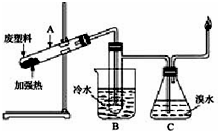 某些废旧塑料隔绝空气加强热,使其变废为宝.其实验装置如图.对某废塑料加强热得到的产物如下表:
某些废旧塑料隔绝空气加强热,使其变废为宝.其实验装置如图.对某废塑料加强热得到的产物如下表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳(固体) |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
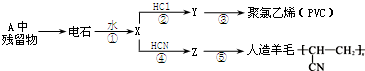
查看答案和解析>>
科目:高中化学 来源: 题型:


| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧杯中有铜无铁 |
| B、烧杯中有铁无铜 |
| C、烧杯中铁、铜都有 |
| D、烧杯中铁、铜都无 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com