解:X、E、G的焰色反应均为黄色,都含有Na元素;
X分解生成无色液体B,故B为H
2O,B

E

G,可知E为NaOH,G为NaAlO
2;
无色气体C与Na
2O
2反应生成白色固体A,C为CO
2,A是Na
2CO
3,2mol白色固体粉末X受热分解,生成白色固体1molNa
2CO
3,1molH
2O,1molCO
2,根据元素守恒可知,X为NaHCO
3,与NaOH反应生成Na
2CO
3,Na
2CO
3
CO
2,CO
2+NaAlO
2→D,D为Al(OH)
3,符合转化关系,NaHCO
3+F→CO
2,F可以是酸或铝盐等,
(1)由上述分析可知,A为Na
2CO
3;
故答案为:Na
2CO
3;
(2)NaHCO
3受热分解生成碳酸钠、二氧化碳、水,反应方程式为:2NaHCO
3
Na
2CO
3+CO
2↑+H
2O;
故答案为:2NaHCO
3
Na
2CO
3+CO
2↑+H
2O;
(3)X+E→A是NaHCO
3与NaOH反应生成Na
2CO
3、H
2O,反应离子方程式为:HCO
3-+OH
-=CO
32-+H
2O;
故答案为:HCO
3-+OH
-=CO
32-+H
2O;
(4)C为CO
2,与Na
2O
2反应为2Na
2O
2+2CO
2=2Na
2CO
3+O
2,反应中O元素化合价由-1价降低为-2价,由-1升高为0价,Na
2O
2既是氧化剂又是还原剂,各占

,0.2molNa
2O
2完全反应转移电子物质的量为0.2mol×

×2=0.2mol,转移电子数目为:0.2mol×N
Amol
-1=0.2N
A;
故答案为:2Na
2O
2+2CO
2=2Na
2CO
3+O
2,0.2N
A.
分析:X、E、G的焰色反应均为黄色,都含有Na元素;
X分解生成无色液体B,故B为H
2O,B

E

G,可知E为NaOH,G为NaAlO
2;
无色气体C与Na
2O
2反应生成白色固体A,C为CO
2,A是Na
2CO
3,2mol白色固体粉末X受热分解,生成白色固体1molNa
2CO
3,1molH
2O,1molCO
2,根据元素守恒可知,X为NaHCO
3,与NaOH反应生成Na
2CO
3,Na
2CO
3
CO
2,CO
2+NaAlO
2→D,D为Al(OH)
3,符合转化关系,NaHCO
3+F→CO
2,F可以是酸或铝盐等.
点评:以无机框图题的形式考查Na、Al等元素单质及化合物的相互转化关系、常用化学用语书写、氧化还原反应计算等,难度中等,无色液体B,X、E、G的焰色反应均为黄色等是解题突破口,结合气体C与Na
2O
2反应利用顺推法与逆推法进行推断,对学生的逻辑推理能力提出较高的要求.


 E
E G,可知E为NaOH,G为NaAlO2;
G,可知E为NaOH,G为NaAlO2; CO2,CO2+NaAlO2→D,D为Al(OH)3,符合转化关系,NaHCO3+F→CO2,F可以是酸或铝盐等,
CO2,CO2+NaAlO2→D,D为Al(OH)3,符合转化关系,NaHCO3+F→CO2,F可以是酸或铝盐等, Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O; Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O; ,0.2molNa2O2完全反应转移电子物质的量为0.2mol×
,0.2molNa2O2完全反应转移电子物质的量为0.2mol× ×2=0.2mol,转移电子数目为:0.2mol×NAmol-1=0.2NA;
×2=0.2mol,转移电子数目为:0.2mol×NAmol-1=0.2NA; E
E G,可知E为NaOH,G为NaAlO2;
G,可知E为NaOH,G为NaAlO2; CO2,CO2+NaAlO2→D,D为Al(OH)3,符合转化关系,NaHCO3+F→CO2,F可以是酸或铝盐等.
CO2,CO2+NaAlO2→D,D为Al(OH)3,符合转化关系,NaHCO3+F→CO2,F可以是酸或铝盐等.

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
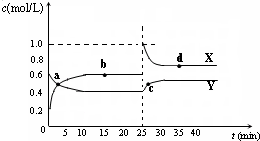 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.