
【题目】下列叙述中,正确的是
A.含金属元素的离子不一定都是阳离子
B.在氧化还原反应中,非金属单质一定是氧化剂
C.最高价含氧酸一定具有强氧化性
D.金属阳离子被还原一定得到金属单质
科目:高中化学 来源: 题型:
【题目】下列物质的制备方法正确的是
A.氯化铝溶液和硫化钠溶液反应制备A12S3
B.用镁粉和空气反应制备Mg3N2
C.用铝粉和MnO2制得锰
D.用电解熔融氯化铝的方法制得单质铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的一组是
A.Mg2+、Al3+、Cl-、OH-
B.Na+、Ba2+、OH-、SO42—
C.K+、Na+、NO3—、HCO3—
D.K+、NH4+、CO32—、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,2.24L苯含有的分子数为0.1NA
B.标准状况下,11.2L乙烷中含有共价键的数目为3NA
C.常温下,1mol羟基中含有的电子数为9NA
D.1mol冰醋酸和1mol乙醇在浓硫酸加热下充分反应生成H2O个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有通式均为(CH2O)n的六种有机物,性质如下:
①A是无色有刺激性的气体,可发生银镜反应
②B、C、D的式量均为A的2倍,E的式量的是A的3倍,F的式量是A的6倍
③B、E的水溶液可使紫色石蕊试液变红,还可与乙醇在一定条件下酯化
④E结构中含有—CH3,两分子E 可形成环状酯
⑤C不溶于水,D、F二种物质的水溶液均呈中性,C既能水解,又能发生银镜反应,D不能发生水解反应,却能发生银镜反应,还能与钠反应放出H2,F能发生银镜反应,淀粉水解可得F。
(1)请推断各物质的结构简式:
A ______________、 B__________________、 C ______________、D_______________、 E__________________、 F________________。
(2)请分别写出符合下列要求的E的同分异构体的结构简式:
①能发生银镜反应和酯化反应,又能发生水解反应 ;
②能发生银镜反应和酯化反应,不能发生水解反应 ;
(3)写出A发生银镜反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从结构的角度可以帮助我们更好的理解有机物的化学性质。
(1) 乙炔是一种重要的化工原料,将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为____________。乙炔与氢氰酸反应可得丙烯腈H2C=CH-C≡N。丙烯腈分子中碳原子轨道杂化类型是____________。[Cu(NH3)2]Cl的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式______________________。
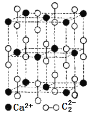
(2)实验室制乙炔使用的电石主要含有碳化钙,写出碳化钙的电子式______________, CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中有哑铃形![]() 的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的
的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的![]() 数目为____________。已知CaC2晶体的密度为2.22g/cm3,该晶胞的体积为____________cm3
数目为____________。已知CaC2晶体的密度为2.22g/cm3,该晶胞的体积为____________cm3
(3) 甲醇催化氧化可得到甲醛,甲醛分子中的键角大约为____________,甲醇的沸点比甲醛的高,其主要原因是_____________________。
(4)已知苯酚具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子为![]() 判断相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是___。
判断相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组依据反应AsO43-+2I-+2H+![]() AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
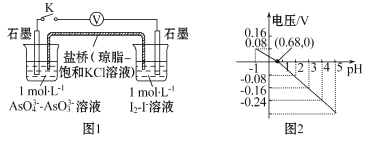
A.调节pH可以改变反应的方向
B.pH=0.68时,反应处于平衡状态
C.pH=5时, 负极电极反应式为2I--2e -= I2
D.pH>0.68时,氧化性I2>AsO43-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,饱和NaClO溶液的pH约为11。某消毒液的主要成分为NaClO,洁厕灵主要成分为HCl。下列解释相关事实的离子方程式中不合理的是
A.该消毒液加白醋生成HClO,可增强消毒能力:H++ClO-=HClO
B.该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-=ClO-+Cl-+H2O
C.常温下,该消毒液的pH≈11,是因为:ClO-+H2O![]() HClO+OH-
HClO+OH-
D.该消毒液与洁厕灵混用会引起中毒:2H++Cl-+ClO-=Cl2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com