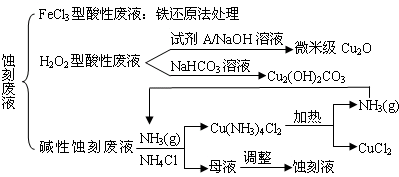
解:(1)FeCl3型酸性废液中含有Fe3+和Fe2+,Fe3+具有氧化性,可与Fe反应,离子方程式为Fe+2Fe3+=3Fe2+,Fe2+具有还原性,可与Cl2反应,离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:Fe+2Fe3+=3Fe2+;2Fe2++Cl2=2Fe3++2Cl-;
(2)H2O2在酸性条件下具有强氧化性,可氧化Cu生成CuCl2,反应的化学方程式为Cu+2HCl+H2O2=CuCl2+2H2O,
故答案为:Cu+2HCl+H2O2=CuCl2+2H2O;
(3)HCl-H2O2型蚀刻液含有Cu2+,在碱性条件下生成Cu(OH)2,可与弱还原剂生成Cu2O,选项中葡萄糖和甲醛都可,但葡萄糖资源广,无害,最合适,故答案为:③;
(4)当温度高于80℃时,Cu2(OH)2CO3易分解生成黑色CuO,导致产品颜色发暗,
故答案为:温度高会使产物部分分解产生黑色的氧化铜导致产品颜色发暗;
(5)Cu2+易与NH3发生反应生成配合物Cu(NH3)4Cl2,促使溶液中Cu(NH3)4Cl2结晶析出,故答案为:促使溶液中Cu(NH3)4Cl2结晶析出.
分析:(1)FeCl3型酸性废液中含有Fe3+和Fe2+,Fe3+具有氧化性,可与Fe反应,Fe2+具有还原性,可与Cl2反应;
(2)H2O2在酸性条件下具有强氧化性,可氧化Cu生成CuCl2;
(3)HCl-H2O2型蚀刻液含有Cu2+,在碱性条件下生成Cu(OH)2,可与弱还原剂生成Cu2O;
(4)当温度高于80℃时,产品颜色发暗,生成黑色CuO;
(5)Cu2+易与NH3发生反应生成配合物Cu(NH3)4Cl2.
点评:本题考查含铜工业废液的处理,题目难度中等,本题考查较为综合,答题时注意把握题给信息,结合元素化合物知识解答.