
下面有关氧化还原反应的叙述不正确的是 ( )
A.氧化还原反应的本质是电子的转移
B.在氧化还原反应中,失去电子的物质,一定有元素化合价升高
C.肯定有一种元素被氧化,另一种元素被还原
D.在反应中不一定所有元素的化合价都发生变化
科目:高中化学 来源:2013-2014江苏省2013-2014学年高三模拟考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离出的c(H+)·c(OH-)=10-22的溶液:K+、Na+、SO42-、S2O32-
B.澄清透明溶液:Mg2+、Cu2+、Cl-、SO42-
C.使酚酞变红色的溶液:NH4+、K+、AlO2-、NO3-
D.含0.1mol·L-1 KI的溶液:Fe3+、Na+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市雨花区高一下学期期末考试化学试卷(解析版) 题型:选择题
诗句“春蚕到死丝方尽,蜡烛成灰泪始干”中“丝”和“泪”分别指
A.纤维素、油脂 B.蛋白质、烃类
C.淀粉、油脂 D.蛋白质、硬化油
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市雨花区高一下学期期末考试化学试卷(解析版) 题型:选择题
“绿色化学”追求化工生产对环境零污染,下列物质中可以称为“绿色氧化剂”的是
A.浓硫酸 B.氯气 C.双氧水 D.漂白粉
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏宿迁市高一下学期期末测试化学试卷(解析版) 题型:选择题
阿伏加德罗常数约为6.02×1023 mol-1,下列说法中正确的是
A.4 g重水(D2O)中所含质子数为0.2×6.02×1023
B.4.48 L N2与CO的混合物所含分子数为0.2×6.02×1023
C.6.2 g白磷与红磷的混合物中所含磷原子数为0.2×6.02×1023
D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏宿迁市高一下学期期末测试化学试卷(解析版) 题型:选择题
与22gCO2所含分子数相等的水的质量为( )
A.44g B.22g C.18g D.9g
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏宿迁市高一下学期期末测试化学试卷(解析版) 题型:选择题
某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,则这种烃可能是( )
①分子中含有7个碳原子的芳香烃 ②分子中含有4个碳原子的烷烃 ③分子中含有12个氢原子的烷烃 ④分子中含有8个碳原子的烷烃( )
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市下学期高二年级期末考试化学试卷(解析版) 题型:填空题
(5分)H2可以催化还原NO以达到消除污染的目的:
(1)已知:①

②

则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式为: ________________。
(2)一定条件下,在体积为2 L的容器中通入1 mol H2和l mol NO气体生成N2(g)和H2O(l),该反应达平衡时,容器内的压强是反应起始时的40%。保持其它条件不变,只往容器中再通入1 mol H2,计算反应再达新平衡时,化学平衡常数为__________。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东肇庆市毕业班第二次模拟考试理综化学试卷(解析版) 题型:填空题
.(17分)减少污染、保护环境是全世界最热门的课题。
(1)为了减少空气中SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)==H2O(g) ΔH1=-241.8 kJ·mol-1
C(s)+1/2O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1
则焦炭与水蒸气反应生成CO的热化学方程式为 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是 (填序号):
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(2)CO在催化剂作用下可以与H2反应生成甲醇:CO(g)+2H2(g) 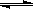 CH3OH(g)。在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如右图所示。
CH3OH(g)。在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如右图所示。

①M、N两点平衡状态下,容器中总物质的物质的量之比为:n(M)总:n(N)总= 。
②若M、N、Q三点的平衡常数KM、KN、KQ的大小关系为 。
(3)催化硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化硝化法中,用H2将NO 还原为N2,一段时间后,溶液的碱性
还原为N2,一段时间后,溶液的碱性
明显增强。则该反应离子方程式为 。
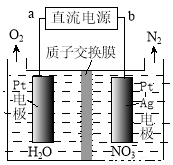
②电化学降解NO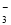 的原理如图所示,电源正极为 (填“a”或“b”);
的原理如图所示,电源正极为 (填“a”或“b”);
若总反应为4NO3-+4H+通电5O2↑+2N2↑+2H2O,则阴极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com