
����Ŀ��20��ʱ��10mL0.1mol��L-1������Һ�в��ϵ���0.1mol��L-1NaOH��Һ����ҺpH�仯��ͼ��ʾ���˹�������Һ������Ũ�ȵĹ�ϵ�������
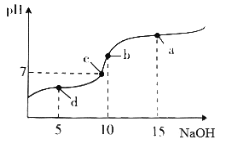
A. a�㣺c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. b�㣺 c(H+)= c(CH3COOH)+c(OH-)
C. c�㣺c(Na+)= c(CH3COO-)>c(H+)=c(OH-)
D. d�㣺c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
���𰸡�B
��������A��a��ΪNaOH��CH3COONa�Ļ�����2c��NaOH��=c��CH3COONa������Һ�ʼ��ԣ����������ˮ�ˮ��̶Ƚ�С��������Һ������Ũ�ȴ�С˳����c��Na+����c��CH3COO-����c��OH-����c��H+������A��ȷ��B��b��ʱ����Һ�ʼ��ԣ�Ӧ��c��H+����c��OH-������B����C��������Һ����غ��֪��Һ��Ӧ����c��Na+��+c��H+��=c��CH3COO-��+c��OH-������Һ�����ԣ�Ӧ��c��H+��=c��OH-������c��Na+��=c��CH3COO-����������Һ������Ũ�ȹ�ϵ��c��Na+��=c��CH3COO-����c��H+��=c��OH-������C��ȷ��D��d��ʱ�����������ҺΪCH3COOH��CH3COONa�Ļ�����Һ�����ԣ�����c��H+����c��OH-������Һ�ʵ����ԣ�c��Na+��+c��H+��=c��CH3COO-��+c��OH-��������c��Na+����c��CH3COO-������c��CH3COO-����c��Na+����c��H+����c��OH-������D��ȷ����ѡB��


 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Fe3+��Fe2+��Mg2+��NH4+��ˮ��Һ�У�����������Na2O2���壬��ַ�Ӧ���ټ��������ϡ���ᣬ����������Ŀû�����Ա仯���ǣ� ��
A.Fe2+
B.NH4+
C.Fe3+
D.Mg2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�Ļ�ѧ����ʽ�����ӷ���ʽ��д��ȷ���� (��)
A. �Ҵ���Ũ�����ϼ�����140�棺![]()
B. 1-��������������Ƶ��Ҵ���Һ���ȣ�![]()
C. ��������Һ��ͨ��������CO2��
D. ��ȩ�ڼ��������±����Ƶ�������ͭ������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���С��Ϊ��̽��ʯ����(17��̼���ϵ�Һ̬���������)�ֽ����������ϩ���ڣ����������ʵ�鷽����
������ʯ���͵�ʯ������Ӳ���Թܵĵײ����Թ��м������Ƭ�������Ƭ��ǿ�ȣ�ʯ��������ͨ�����ȵ����Ƭ���棬������Ӧ�õ�����������ͨ��ʢ��ij�Լ����Թ��м�����֤(װ����ͼ��ʾ)��

�ش��������⣺
(1)������ϩ���ʵĹ�������______________��
(2)��֤�����������к�����ϩ��ʵ�鷽����______________________________��
(3)��֤�����������к�����ϩ��ʵ��������______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ϩ(CH2 =CH2)��˵������ȷ����
A. ��ϩ������2��̼ԭ�Ӷ���sp2�ӻ�B. ��ϩ�����д��ڷǼ��Լ�
C. ��ϩ������4��Hԭ����ͬһƽ����D. ��ϩ���Ӿ��������칹
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A�Ǻϳ���Ȼ�ĵ��壬����ʽΪC5H8��A��һϵ�з�Ӧ��ͼ(���ַ�Ӧ������ȥ)

��֪����1��![]()
��2��CH3COOCH2CH3+H2O![]() CH3COOH+CH3CH2OH
CH3COOH+CH3CH2OH
�ش��������⣺
��1��A�Ľṹ��ʽΪ_______��
��2��B�ķ���ʽΪ_______��
��3���ڵķ�Ӧ����ʽΪ_______��
��4���ٺ͢۵ķ�Ӧ���ͷֱ���_____, ______��
��5��CΪ�������������������Ǽ�����ṹ��ʽΪ__________��
��6�������к�������̼̼˫��,������˫��֮����һ��̼̼�����Ĺ����ϩ���뵥ϩ�����ɷ�������A��B֮��ķ�Ӧ����д����Ϊ��Ԫ������M(C6H10)��N(C6H8)�������෴Ӧ�Ļ�ѧ����ʽ____________________��
��7��A��ͬ���칹���в����ۻ���ϩ(C=C��C���ṹ��Ԫ����״������_______�֣�������˳���칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���������ԭ�ӵ��ӻ���ʽ�ͷ��ӵĿռ乹�;���ȷ����
A. C2H2��sp2��ֱ���� B. SO42-��sp3��������
C. BF3��sp2��ƽ�������� D. H3O+��sp3��V��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¶ȷ�Ӧ�ٶȼӿ����Ҫԭ����
A. �����˶��ٶȼӿ�B. �������
C. ��ϵ��������D. ����ӵİٷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�Ļ���������������������������ء�
��1����״���£���11.2LCO2ͨ��100mL 1mol/L��NaOH��Һ�У�������Һ������Ũ���ɴ�С��˳��Ϊ___________������Һ������Ũ�ȷ���������е�ʽ:
��c(OH-)=2c(H2CO3)+______��
��c(H+)+c(Na+)=_________��
��2����ͼ��1mol NO2��1molCO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��___________

��3����һ���¡������ܱ������з�����Ӧ��Ni(s)+4CO(g)![]() Ni(CO)4(g)��
Ni(CO)4(g)��![]() H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99.9���ĸߴ���������˵����ȷ����________ (����ĸ���)��
H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99.9���ĸߴ���������˵����ȷ����________ (����ĸ���)��
A������Ni���������CO��ת���ʣ�Ni��ת���ʽ���
B����С�����ݻ���ƽ�����ƣ�![]() H��С
H��С
C����Ӧ�ﵽƽ�����CO�ٴδﵽƽ��ʱ��CO�������������
D����4v��[Ni(CO)4]=v��(CO)ʱ�������л�������ܶȲ���ʱ������˵����Ӧ�Ѵﻯѧƽ��״̬
��4�������Ѵ���������ķ�Ӧ���̣���Ҫ�������¼�����Ӧ����������Ϊ25�桢1.01��105Pa�ⶨ����
��CH3OCH3(g)+H2O(l)![]() 2CH3OH(l) ��H����24.52kJ/mol
2CH3OH(l) ��H����24.52kJ/mol
��CH3OH(l)+H2O(l)![]() CO2(g)+3H2(g) ��H����49.01kJ/mol
CO2(g)+3H2(g) ��H����49.01kJ/mol
��CO(g)+H2O(l)![]() CO2(g)+H2(g) ��H����41.17kJ/mol
CO2(g)+H2(g) ��H����41.17kJ/mol
��CH3OH(l)![]() CO(g)+2H2(g) ��H����90.1kJ/mol
CO(g)+2H2(g) ��H����90.1kJ/mol
��ҵ�����в�ò�ͬ�¶��¸�������������������ת���ʵĹ�ϵ����ͼ��ʾ��


������Ϊ��Ӧ���Ƶ�����¶�ӦΪ___________��
A��300��350�� B��350��400�� C��400��450�� D��450��500��
�����¶ȴﵽ400���Ժ�������CO2�Լ�����ͬ�ı仯�������Խ��ͣ���CO��H2�������Ҳ�Լ�����ͬ�ı仯�������ߣ��������ܵ�ԭ����___________������Ӧ�Ļ�ѧ����ʽ��ʾ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com