
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/mi n | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
分析 (1)已知:
①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ•mol-1;
②2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1;
根据盖斯定律①-$\frac{1}{2}$②可得;反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度、含量等不再发生变化,以及由此衍生的其它量不变,可由此进行判断;
(2)①根据v=$\frac{△c}{△t}$计算计算v(CO),再利用速率之比等于化学计量数之比计算v(CO2);
②第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO2的物质的量比第一组的一半少,表明该反应为放热反应;
③使实验3达到平衡状态时各物质的体积分数与实验2分别相等,为等效平衡,该反应为反应前后气体的体积不发生变化,满足n(H2O):n(CO)=1:2即可;
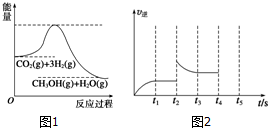
(3)①根据图象知,该反应的正反应是放热反应,能使c(CH3OH)增大,说明平衡向正反应方向移动;
②图示中t2时的逆反应速率加快,根据及影响化学反应速率的因素判断改变的条件.
解答 解:(1)①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ•mol-1;
②2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1;
根据盖斯定律①-$\frac{1}{2}$×②得:C(s)+H2O(g)?CO(g)+H2(g)△H=+131kJ•mol-1;
a.反应前后气体的物质的量发生变化,随反应进行气体的物质的量增加,压强增大,容器中的压强不变,说明反应到达平衡,故正确;
b.l molH-H键断裂的同时断裂2mol H-O键,断裂2mol H-O键同时生成l molH-H键,说明反应到达平衡,故正确;
c.根据反应可知,自始至终v正(CO)=v正(H2O),若v正(CO)=v逆(H2O),则v正(H2O)=v逆(H2O),说明反应到达平衡,故正确;
d.根据反应可知,自始至终c(CO)=c(H2),不能说明反应到达平衡,故错误;
e.容器的容积不变,随反应进行容器内气体的质量增加,所以随反应进行密度增大,容器中气体的密度不变,说明反应到达平衡,故正确;
故答案为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131kJ•mol-1;abce;
(2)①v(CO)=$\frac{(4mol-2.4mol)÷2L}{5min}$=0.16mol•(L•min)-1,速率之比等于化学计量数之,则v(CO2)=0.16mol•(L•min)-1,
故答案为:0.16mol•(L•min)-1;
②实验1中CO的转化率为$\frac{4-2.4}{4}$×100%=40%,实验2中CO的转化率为$\frac{2-1.6}{2}$×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热;
故答案为:吸热;
③使实验3达到平衡状态时各物质的体积分数与实验2分别相等,为等效平衡,该反应为反应前后气体的体积不发生变化,满足n(H2O):n(CO)=1:2即可,即b=2a,且a>1,;
故答案为:b=2a,且a>1;
(3)①a.根据图象知,该反应的正反应是放热反应,升高温度,平衡逆向移动,c(CH3OH)减小,故a错误;
b.充入He(g),使体系压强增大,由于容器为恒容容器,各组分浓度不变,平衡不移动,c(CH3OH)不变,故b错误;
c.将H2O(g)从体系中分离出来,平衡正向移动,c(CH3OH)增大,故c正确;
d.再充入1mol CO2和3molH2,平衡正向移动,c(CH3OH)增大,故d正确;
e.将该密闭容器改为恒压密闭容器,反应是个体积减小的反应,则相对于恒容为加压,正方向移动,c(CH3OH)增大,故e正确;
故答案为:cde;
②根据图象知,t2时,逆反应速率突然增大,原因可能是使用了催化剂、升高了温度、增大了压强、增大了生成物的浓度,而后逆反应速率减小,平衡逆向移动,则只能是t2时增大了生成物的浓度或升高了温度,
故答案为:升高温度(增大生成物CH3OH的浓度).
点评 题考查了反应自发进行的条件、平衡状态的判断、化学反应速率的求算、化学平衡常数的求算、据K随温度的变化判断反应吸热还是放热、等效平衡,题目有一定难度.


科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其他分散系的本质特征是胶体具有丁达尔现象 | |
| B. | NaCl溶液在电流的作用下电离成Na+与Cl- | |
| C. | 2NO2+2NaOH═NaNO3+NaNO2+H2O是氧化还原反应 | |
| D. | 固体NaCl不导电,所以NaCl是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeS的Ksp小于CuS的Ksp | |
| B. | 该反应平衡常数K=$\frac{{K}_{sp}(FeS)}{{K}_{sp}(CuS)}$ | |
| C. | 溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Fe2+)保持不变 | |
| D. | 达到平衡时c(Fe2+)=c(Cu2+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 起始浓度(mol/L) | 1.5 | 1.0 | 0 |
| 2s末浓度(mol/L) | 0.9 | 0.8 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠块沉在乙醇液面的下面 | B. | 钠块熔化成小球 | ||
| C. | 钠块在乙醇的液面上游动 | D. | 钠块表面有气泡产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com