
将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是:
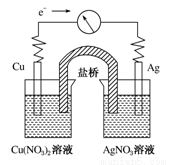
A、KNO3盐桥中的K+移向Cu(NO3)2溶液
B、Cu作负极,发生还原反应
C、电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液
D、工作一段时间后,AgNO3溶液中c(Ag+)减小
 53天天练系列答案
53天天练系列答案科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列各组的电极材料和电解液,不能组成原电池的是
A.铜片、石墨棒,稀硫酸 B.铜片、石墨棒,硝酸银溶液
C.锌片、铜片,稀盐酸 D.铜片、银片,FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二上学期第一次月考化学试卷(解析版) 题型:选择题
根据所学知识判断,下列反应中,在任何温度下都不自发进行的
A.2O3(g)═3O2(g)△H<0
B.2CO(g)═2C(s)+O2(g)△H>0
C.N2(g)+3H2(g)═2NH3(g)△H<0
D.CaCO3(s)═CaO(s)+CO2(g)△H>0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市兖州区高一上学期期中测试化学试卷(解析版) 题型:选择题
在空气中,有下列反应发生:①N2+O2═2NO;②2NO+O2═2NO2; ③3NO2+H2O═2HNO3+NO;④2SO2+O2═2SO3;⑤SO3+H2O═H2SO4;⑥SO2+H2O═H2SO3;⑦3O2═2O3.其中属于氧化还原反应的是
A. ①②③④ B. ①②③④⑦
C. ①②④⑦ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.可利用过滤的方法区别溶液和胶体
B.制备Fe(OH)3胶体通常是将Fe(OH)3固体溶于沸水
C.直径介于1nm~100nm之间的微粒称为胶体
D.电泳现象证明胶体粒子是带电的
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一上学期期中测试化学试卷(解析版) 题型:选择题
0.5 L AlCl3溶液中Cl-为9.03×1022个,则AlCl3溶液的物质的量浓度为
A.0.1 mol·L-1 B.1 mol·L-1 C.3 mol·L-1 D.1.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届广西省高三上学期期中测试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1的CaCl2溶液:Na+、K+、Cl-、CO32-
B.1.0 mol·L-1的HNO3溶液:K+、[Ag(NH3)2]+、Cl-、SO42-
C.1.0 mol·L-1的KI溶液:Na+、Fe3+、Cl-、SO42-
D.澄清透明的溶液:Cu2+、SO42-、Mg2+、Cl-
查看答案和解析>>
科目:高中化学 来源:2016届湖北省襄阳市高三上学期期中测试化学试卷(解析版) 题型:填空题
(1)I.短周期某主族元素M的电离能情况如图(A)所示,则M元素位于周期表的第____族;
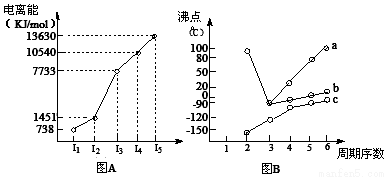
Ⅱ.图B折线c可以表达出第____________族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:________________(填“a”或 “b”);
Ⅲ.部分有机物的熔沸点见下表:
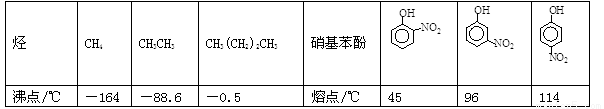
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):____________________;
(2)COCl2俗称光气,分子中C原子采取__________杂化成键;其中碳氧原子之间共价键含有___________(填字母):
a.2个σ键
b.2个π键
c.1个σ键.1个π键;
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为_________________________;
Ⅱ.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的 ,则绿色晶体配合物的化学式为_________________________。
,则绿色晶体配合物的化学式为_________________________。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期10月教学质检理综化学试卷(解析版) 题型:实验题
金属钼(Mo)可以增强合金的某些机械性能和耐腐蚀性。下图是化工生产中制备金属钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):

(1)在灼烧钼矿时发生化学反应:2MoS2+7O2 2MoO3+4SO2,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为______________。
2MoO3+4SO2,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为______________。
(2)步骤①中,灼烧钼矿时,用于盛放固体的仪器的名称为______________。
(3)写出步骤②中发生反应的离子方程式______________________________。
(4)在步骤③中需要加入过量硝酸,检验硝酸过量的操作为_________________。
(5)某同学拟选用如下装置,用氢气还原三氧化钼,同时检验该反应的氧化产物,根据要求回答下列问题。
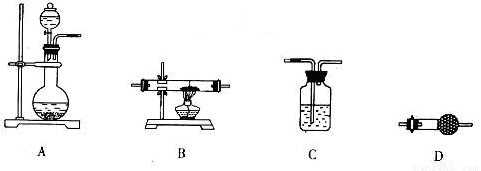
①若两次使用到C装置,则装置D中所盛的药品是___________(填试剂名称)。
②根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞后_________→_________→_________→_________(请按正确的顺序填入下列步骤的代号)。
a.收集气体并检验其纯度 b.停止加热,充分冷却
c.加热反应一段时间 d.关闭分液漏斗活塞,停止通氢气
(6)化学分析中,常用沉淀法测定金属的含量。若称取三氧化钼粗产品m g,用浓氨水溶解后,再滴加足量的硝酸使其完全转化为钼酸沉淀,此时消耗0.2 mol/L HNO3溶液250mL ,则粗产品中三氧化钼的含量为 (请用含m的表达式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com