
| A. | 常温下,0.1mol•L-1 Na2S溶液中存在:c(OH-)=c(H+ )+c(HS-)+c(H2S) | |
| B. | PH=3的醋酸溶液中:c(H+ )=c(CH3COO-)=0.3mol•L-1 | |
| C. | 某溶液中由水电离出的c(OH- )=1×10-a mol•L-1,若a>7时,则该溶液的pH可能为a | |
| D. | pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+ )>c(H+ )>c(OH- ) |
分析 A、根据质子守恒分析解答;
B、氢离子来源于醋酸和水的电离,由此分析解答;
C、25℃时,某溶液中水电离出的[H+]=1×10-amol•L-1,若a>7,水的电离受到抑制,可能是强酸或强碱溶液;
D、pH=12的氨水与pH=2的盐酸中,氨水浓度大于盐酸,等体积混合,氨水过量,溶液呈碱性.
解答 解:A、根据质子守恒,可知:c(OH-)=c(H+ )+c(HS-)+2c(H2S),故A错误;
B、氢离子来源于醋酸和水的电离,所以c(H+ )=0.3mol•L-1>c(CH3COO-),故B错误;
C、25℃时,某溶液中由水电离出的[H+]=1×10-amol•L-1,若a>7,水的电离程度减少,因为它们都会抑制水的电离,所以可能是强酸或强碱溶液,若是强酸,pH为14-a,.若是强碱,pH为a,故C正确;
D、pH=12的氨水与pH=2的盐酸中,氨水浓度大于盐酸,等体积混合,氨水过量,溶液呈碱性,所以c(OH-)>c(H+),溶液中存在电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以得c(NH4+)>c(Cl-),溶液中一水合氨电离程度较小,所以c(Cl-)>c(OH-),则溶液中离子浓度大小顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+),故D错误;
故选C.
点评 本题考查了弱电解质的电离、酸碱混合溶液定性判断、盐的水解等知识点,根据酸碱混合溶液的酸碱性结合电荷守恒来分析解答,比较容易.


科目:高中化学 来源: 题型:解答题
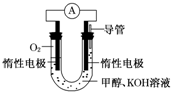 为了解决空气污染危机,中国煤炭业制定了“煤制气”计划.工业上可用煤生产合成气(CO和H2),也可用煤制天然气.
为了解决空气污染危机,中国煤炭业制定了“煤制气”计划.工业上可用煤生产合成气(CO和H2),也可用煤制天然气.| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
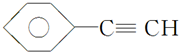 B.CH4
B.CH4查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO${\;}_{3}^{2-}$ | B. | CH3COO- | C. | Fe2+ | D. | Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com