
| A. | pH=4 | B. | c(H+)=0.001 mol•L-1 | ||
| C. | c(OH- )=1×10-11 mol•L-1 | D. | c(H+):c(OH- )=1×104 |
分析 溶液中氢离子浓度越大,该溶液的酸性越强,则酸性最弱的溶液中含有氢离子浓度最小,据此对各选项进行判断.
解答 解:A.pH=4的溶液中氢离子浓度为1×10-4mol•L-1;
B.c(H+)=0.001 mol•L-1=1×10-3mol•L-1;
C.c(OH- )=1×10-11mol•L-1的溶液中氢离子浓度为:1×10-3mol•L-1;
D.c(H+):c(OH- )=1×104,结合水的离子积c(H+)•c(OH- )=1×10-14可知氢离子浓度为1×10-5mol•L-1;
氢离子浓度越大,溶液酸性越强,各选项中氢离子浓度最小的为D,则酸性最弱的为D,
故选D.
点评 本题考查了溶液酸性强弱比较,题目难度不大,明确溶液酸碱性与溶液中氢离子浓度大小为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:选择题
| A. | AgCl沉淀生成和溶解同时在不断进行,且速率相等 | |
| B. | AgCl难溶于水,则溶液中没有Ag+和Cl- | |
| C. | 只要向含有AgCl的饱和溶液中加入盐酸,一定会有沉淀生成 | |
| D. | 向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀不变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
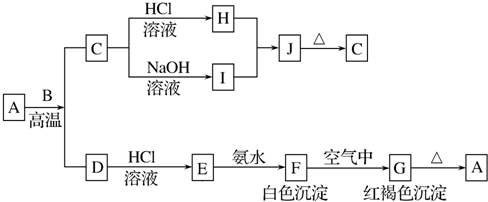
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图Ⅰ可能是不同压强对反应的影响,且p2>p1,a+b<n | |
| B. | 图Ⅱ可能是不同压强对反应的影响,且p1>p2,n=a+b | |
| C. | 图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好 | |
| D. | 图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 元素周期表中前两周期的六种元素X、Y、Z、M、N、Q原子序数依次增大,六种元素价电子数之和为26,原子半径依Y、Z、M、N、Q、X依次减小.依据信息,回答下列问题:
元素周期表中前两周期的六种元素X、Y、Z、M、N、Q原子序数依次增大,六种元素价电子数之和为26,原子半径依Y、Z、M、N、Q、X依次减小.依据信息,回答下列问题: .
.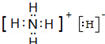 ,常温下A与水反应的化学方程式为NH4H+H2O=NH3•H2O+H2↑.
,常温下A与水反应的化学方程式为NH4H+H2O=NH3•H2O+H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com