
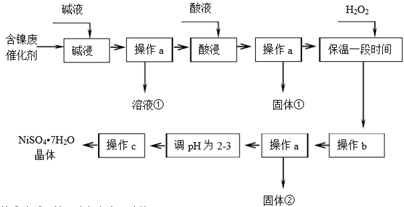
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| ��ʼ����pH | 3.8 | 2.7 | 7.6 | 7.1 |
| ��ȫ����pH | 5.2 | 3.2 | 9.7 | 9.2 |
���� ��1�����ݷ��ϳɷ�֪�����������������Ӧ����Һ�к���ƫ��������ӣ�
��2���������ݱ�֪��Ӧ����������ת���������ӳ�ȥ������˫��ˮ���������������������ӣ������������ʣ���Ư��Һ����Ҫ�ɷִ������ƣ����������������˫��ˮ�����������ʣ����������˫��ˮ��
��3��������ҺpHʹFe3+��ȫ������ʹNi2+�����������������������������
��4�����ˡ���������Ҫ�ò�������������������������������ˮ���ڽᾧ�����У�����������ˮ�⣬������Һ��ǿ���ԣ�����������ˮ�⣻
��5���������˫��ˮ���㣬��Ӧʱ��϶̣��������Ӳ�����ȫת���������ӣ���Ʒ�л���������������壬����Fe2+�Լ���������ˮ��KSCN��Һ�����Ը��������Һ�ȣ�
��6���������ӷ�Ӧ����ʽ��Ni2++H2Y2-=NiY2-+2H+���г���ϵʽ���㼴�ɣ�
��� �⣺��1������������������ܷ�Ӧ����Һ�к��еĺ��н�����������ƫ��������ӣ��ʴ�Ϊ��AlO2-��
��2���������Ӿ��л�ԭ�ԣ�˫��ˮ���������ԣ�����˫��ˮ��Ϊ�������������ӳ�Ϊ�����ӣ����ӷ�Ӧ����ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O��Ư��Һ����Ҫ�ɷִ������ƣ����������������˫��ˮ�����������ʣ��ʴ�����Լ�Ϊ�������ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��A��
��3���ɱ����֪�����������ij�����ΧΪ��2.7-3.2�������ӵij�����Χ��7.1-9.2������pH��3.2-7.1��Ŀ���dz�ȥ�����ӣ����Dz����������ӣ��ɣ�2����֪������b������Һ��ΧΪ3.2-7.1����ô��ʱ�õ��ij����������������ʴ�Ϊ����ȥFe3+�� Fe��OH��3��
��4������a�ǹ��˵õ��������Һ��c������Ũ���õ�������˵õ�NiSO4•7H2O������a��c�о���ʹ�õ�����Ϊ��������������ˮ������ԣ���Һʼ�ձ������Կ���������ˮ�⣬�ʴ�Ϊ����������������Һ�����ԣ�
��5���������˫��ˮ���㣬��Ӧʱ��϶̣��������Ӳ�����ȫ�������������ӣ���Ʒ�л����̷����������ӿ��Ա�����Ϊ�����ӣ�����������������֤����ȷ�ķ����ǣ�ȡ������Ʒ��������ˮ���μ����Ը��������Һ������Һ��ɫ��ȥ�����Ʒ�к����������ӣ��ʴ�Ϊ����Ʒ�л����̷���ȡ������Ʒ��������ˮ���μ����Ը��������Һ������Һ��ɫ��ȥ�����Ʒ�к����������ӣ�
��6��n��Na2H2Y��=0.2mol/L��34.5��10-3L=6.9��10-3mol�����ݵζ���Ӧʽ֪��m��NiSO4•7H2O��=6.9��10-3mol��281g/L=1.94g���أ�NiSO4•7H2O��=$\frac{1.9400g}{2.0000g}$��100%=97.0%���ʴ�Ϊ��97.0%��
���� ���⿼����������Ʊ����̣��漰���ӷ�Ӧ����ʽ��д��������ԭ��Ӧ�����ӵ���֤�ȣ������ۺ��Խ�ǿ���ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҷ����ͱ�������Ϊͬϵ�� | |
| B�� | ����ʽΪC7H80�����ڷ������ʵ�ͬ���칹����4�� | |
| C�� | �ױ���ʹ���Ը��������Һ��ɫ��˵����ʹ��������� | |
| D�� | ���������������������ʿɼӱ���Na2C03��Һ��Һ��ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ѹǿ����������ʵ��ͻ�ѧʵ��������ҪӰ�죮
����ѹǿ����������ʵ��ͻ�ѧʵ��������ҪӰ�죮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 25�� | pH | 25�� | pH |
| ����H2S��Һ | 3.9 | FeS��ʼ���� | 3.0 |
| SnS������ȫ | 1.6 | FeS������ȫ | 5.5 |
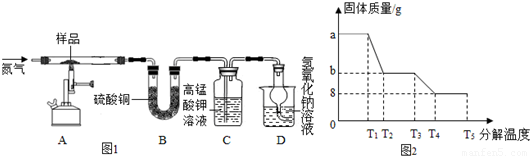
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
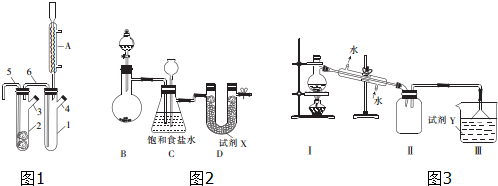
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
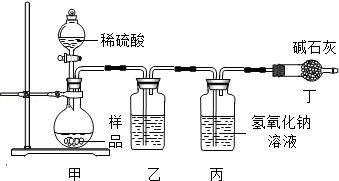
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Cu��OH��2��Һ�ɼ����Ҵ�����ȩ�����ᡢ����������ɫ��Һ | |
| B�� | ����ˮ�Ҵ��������ᡢ3mol/L�������������� | |
| C�� | ������ˮ�����ۻ���Ƴ��屽 | |
| D�� | ���÷�Һ©��������ͺ�ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com