
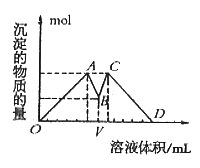
| A.混合溶液中c(AlCl3):c(MgCl2)=1:1 |
| B.混合溶液中c(AlCl3):c(MgCl2)=3:1 |
| C.V之前加NaOH溶液,V之后加盐酸 |
| D.这种盐酸与NaOH溶液中溶质的物质的量浓度相同 |


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:不详 题型:单选题
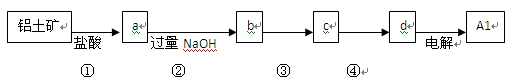
| A.①、②中除加试剂外。还需要进行过滤操作 |
| B.a 、b中铝元素的化合价相同 |
| C.③中需要通入过量的氨气 |
| D.④进行的操作是加热,而且d 一定是氧化铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
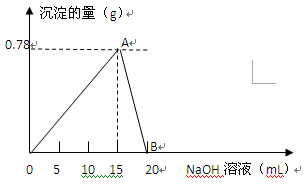
| A.先生成沉淀,后沉淀全部溶解 |
| B.当溶液中Al3+全部沉淀出来时,沉淀的总物质的量最大 |
| C.最后得到的沉淀是BaSO4 |
| D.最后的沉淀为2mol BaSO4、1mol Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝的氧化物粉末是白色的,属于两性氧化物;铁、铜的最高价氧化物粉末都是黑色的,属于碱性氧化物 |
| B.铝制品、铁制品、铜制品长期放置在空气中均易腐蚀 |
| C.制备AlCl3、FeCl3、CuCl2均能采用单质与氯气反应的方法 |
| D.常温下Cu、Fe、Al均不能和浓硫酸发生化学反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.7g | B.3.6g | C.4.8g | D.7.2g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
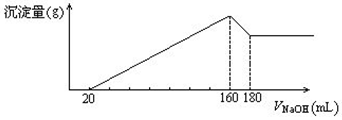
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com