
 如图,C、D,E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色.则下列说法正确的是( )
如图,C、D,E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色.则下列说法正确的是( )| A、若用乙烷、空气燃料电池作电源,电解质为KOH溶液,则B极的电极反应式为:02+2H20+4e-=40H- |
| B、欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 |
| C、(丁)装置中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷 |
| D、C、D、E、F电极均有单质生成,其物质的量比为1:2:2:2 |


 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
| A、2个 | B、3个 | C、4个 | D、5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图①装置可验证酸性:H2CO3>H2SiO3 |
| B、图②装置可用于收集气体H2、CO2、Cl2、NH3 |
| C、图③装置可用于分离互不相溶的两种液体 |
| D、图④装置可制备Fe(OH)2并能较长时间保持其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解MgCl2饱和溶液,可制得金属镁 |
| B、用食醋去除水壶中的水垢所发生的是水解反应 |
| C、在海轮外壳上镶入不活泼的铜块,可减缓船体的腐蚀速率 |
| D、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用作净化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
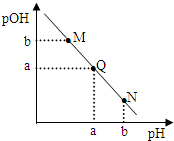 某温度下,向一定体积的0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的关系如图[已知:pOH=-lgc(OH-)],下列说法正确的是
某温度下,向一定体积的0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的关系如图[已知:pOH=-lgc(OH-)],下列说法正确的是| A、M点溶液导电能力强于Q点溶液导电能力 |
| B、N点所示溶液中,c(CH3COO-)>c(Na+) |
| C、M点与N点所示溶液中水的电离程度相等 |
| D、Q点消耗NaOH溶液体积等于醋酸溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明该溶液中一定含有SO42- |
| B、某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 CO32-或 HCO3- |
| C、某溶液中加盐酸产生刺激性气味的无色气体,该气体能使品红溶液褪色,说明该溶液中一定含有SO32- |
| D、取少量久置的Na2SO3样品于试管中加水溶解,再加入足量盐酸有气体产生,然后加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、未冷却即转移、定容 |
| B、未洗烧杯及玻璃棒 |
| C、定容时俯视刻度线观察液面 |
| D、容量瓶中原有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com