
250mL 0.01mol·L-1的NaOH溶液,在空气中放置相当长时间后,用已知浓度的稀H2SO4溶液滴定.若用甲基橙作指示剂,设消耗H2SO4溶液体积为VA;若用酚酞作指示剂,设消耗H2SO4溶液体积为VB,则VA与VB的关系为
[ ]
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:阅读理解
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) |
滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 20.02 | 20.00 |
| 2 | 0.10 | 20.00 | 20.00 |
| 3 | 0.10 | 19.00 | 20.00 |
| 4 | 0.10 | 19.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
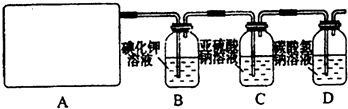
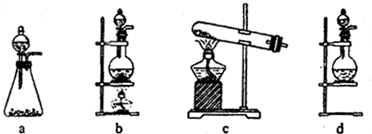
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
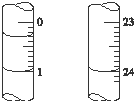
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 复方氢氧化铝 | 盐酸雷尼替丁 | |||
| 滴定前 | 滴定后 | 滴定前 | 滴定后 | |
| 1 | 0.01 | 79.8 | 0.02 | 18.6 |
| 2 | 0.00 | 79.5 | 0.03 | 19.0 |
| 3 | 0.03 | 80.5 | 0.00 | 18.7 |
| 时间(min) | 0 | 0.5 | 1 | 1.5 | 2 | 2.5 | 3 | 3.5 | 4 | 5 |
| 复方氢氧化铝 | 3.53 | 3.62 | 3.70 | 3.75 | 3.79 | 3.84 | 3.88 | 3.89 | 3.90 | 3.92 |
| 盐酸雷尼替丁 | 1.72 | 1.65 | 1.60 | 1.55 | 1.74 | 1.80 | 1.84 | 1.87 | 1.87 | 1.88 |
| 时间(min) | 10 | 15 | 20 | 25 | 30 | 35 | 40 | |||
| 复方氢氧化铝 | 3.97 | 4.01 | 4.12 | 4.13 | 4.14 | 4.15 | 4.15 | |||
| 盐酸雷尼替丁 | 1.88 | 1.87 | 1.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 现象与结论 |
| 步骤1:向试管中加入少量固体产物,再加入足量 |
若溶液颜色明显改变,且有 |
| 步骤2:将步骤1中得到的浊液过滤,并用蒸馏水洗涤至洗涤液无色 | |
| 步骤3:取步骤2得到的少量固体与试管中,滴加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com