
| A. | pH=1的KHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| B. | CH3COONa和BaCl2混合溶液:c(Na+)+c(Ba2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| C. | 三种相同浓度的铵盐溶液中c(NH4+)从大到小的顺序:NH4HSO4、NH4Cl、NH4HCO3 | |
| D. | 已知AgCl、AgBr、AgI溶度积常数依次为1.6×l0-10、7.7×10-13、8.7×10-17,则对应饱和溶液中c(X-)从大到小的顺序为:Cl-、Br-、I- |
分析 A.根据KHSO4溶液中的电荷守恒及物料守恒分析;
B.根据CH3COONa和BaCl2混合溶液中的物料守恒判断;
C.硫酸氢铵中氢离子抑制了铵根离子的水解,碳酸氢根离子促进了铵根离子的水解;
D.化学式相似的物质的溶度积常数越小,物质越难溶,据此分析三种离子浓度大小.
解答 解:A.pH=1的KHSO4溶液中,硫酸氢钾完全电离,根据电荷守恒可知:c(Na+)+c(H+)=2c(SO42-)+c(OH-),根据物料守恒可得:c(Na+)=c(SO42-),二者结合可得:c(H+)=c(SO42-)+c(OH-),故A正确;
B.CH3COONa和BaCl2混合溶液中,根据物料守恒可得:c(Na+)c(CH3COO-)+c(CH3COOH)、2c(Ba2+)=2c(Cl-),二者结合可得:c(Na+)+2c(Ba2+)=c(CH3COO-)+c(CH3COOH)+c(Cl-),故B错误;
C.NH4HSO4电离出的氢离子抑制了铵根离子的水解,其溶液中铵根离子浓度最大;NH4HCO3中碳酸氢根离子水解促进了铵根离子的水解,其溶液中铵根离子浓度最小,则三种相同浓度的铵盐溶液中c(NH4+)从大到小的顺序为:NH4HSO4>NH4Cl>NH4HCO3,故C正确;
D.化学式相似的物质的溶度积常数越小物质越难溶,常温下在水中溶解能力为AgCl>AgBr>AgI,则对应饱和溶液中c(X-)从大到小的顺序为:Cl-、Br-、I-,故D正确;
故选B.
点评 本题考查离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒及盐的水解原理即可解答,注意掌握判断离子浓度大小常用方法,试题培养了学生的分析能力及综合应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 煤制乙醇,有利于保护环境,实现能源充分利用 | |
| B. | 煤制乙醇可缓解靠发酵产生乙醇导致的“与人类争粮”的局面 | |
| C. | 等物质的量的乙醇.汽油完全燃烧,乙醇放出的热量多 | |
| D. | 乙醇是世界公认的优良汽油添加剂,可有效改善汽油品质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
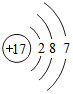 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.8g正丁烷与异丁烷组成的混合气体中含有的C-H键数目为NA | |
| B. | 1mol的CO2和水蒸气的混合气体与过量Na2O2充分反应转移的电子数为2NA | |
| C. | 将0.2molNH3充入密闭容器中在一定条件下加热分解,生成N2的分子数为0.1NA | |
| D. | 相同温度下50mL0.1mol•L-1CH3COOH溶液和10mL0.5mol•L-1CH3COOH溶液中所含CH3COOH分子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
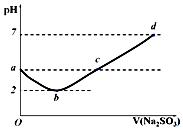 常温下向某浓度的氯水中逐滴滴入Na2SO3溶液,无气体逸出,溶液pH变化如图所示,下列关系错误的是( )
常温下向某浓度的氯水中逐滴滴入Na2SO3溶液,无气体逸出,溶液pH变化如图所示,下列关系错误的是( )| A. | a点:c(H+)>c(Cl-)>c(ClO-) | |
| B. | b点:$\frac{1}{2}$ c(Cl-)=c(SO42-)=0.005 mol•L-1 | |
| C. | c点:c(Na+)=2c(HSO3-)+2c(SO32-)+2c(SO42-) | |
| D. | d点:c(Na+)=c(Cl-)+2c(SO32-)+c(HSO3-)+2c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 交换膜Ⅰ为阴离子交换膜,A-从浓缩室通过向阳极移动 | |
| B. | 交换膜Ⅱ为阴离子交换膜,H+从浓缩室通过向阴极移动 | |
| C. | 阳极的电极反应式为2H2O-4e-═4H++O2↑ | |
| D. | 400mL0.1mol•L-1乳酸溶液通电一段时间后,浓度上升到0.6mol•L-1,则阴极上产生的H2在标准状况下的体积为4.48L |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z、W、Q、X、Y原子半径依次减小 | |
| B. | W最高价氧化物对应水化物一定能溶于Z最高价氧化物对应水化物的溶液中 | |
| C. | Y与Q形成化合物在常温下一定为气态 | |
| D. | Z、Q元素的单质都可以将X元素的单质从其氧化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向甲、乙、丙三个恒容密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).相关数据如表,反应过程中C的浓度随时间变化关系如图.下列说法正确的是( )
向甲、乙、丙三个恒容密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).相关数据如表,反应过程中C的浓度随时间变化关系如图.下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6 mol A 2 mol B |
| A. | T1>T2,x=1 | |
| B. | T2℃时,该反应的平衡常数为0.8 | |
| C. | A的平衡转化率a(甲):a(乙)=2:3 | |
| D. | 15~20min内C的平均反应速率v(乙)<v(丙) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com