
 .
.分析 X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,X原子的最外层电子数是次外层电子数的3倍,则原子核各层电子分别为2、6,故X为O元素,X、M同主族,则M为S元素,Y在同周期主族元素中原子半径最大,故Y、Z、M、N处于第三周期,Y为Na元素,N为Cl元素,Z和Cl可以形成ZCl2型化合物,Z为+2价,故Z为Mg元素,结合对应的单质化合物的性质与元素周期律的递变规律解答.
解答 解:X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,X原子的最外层电子数是次外层电子数的3倍,则原子核各层电子分别为2、6,故X为O元素,X、M同主族,则M为S元素,Y在同周期主族元素中原子半径最大,故Y、Z、M、N处于第三周期,Y为Na元素,N为Cl元素,Z和Cl可以形成ZCl2型化合物,Z为+2价,故Z为Mg元素,
(1)N为Cl元素,在周期表中的位置是第三周期第ⅤⅡA族,Cl的最高价氧化物的化学式为Cl2O7,
故答案为:第三周期第ⅤⅡA族;Cl2O7;
(2)由元素X、Y形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为过氧化钠,过氧化钠中含有的化学键类型为离子键和非极性键,用电子式表示过氧化钠的形成过程为 ,
,
故答案为:离子键和非极性键; ;
;
(3)M为S元素,Y为Na元素,Y、M两种元素对应的最高价氧化物的水化物分别为硫酸和氢氧化钠,它们相互反应的离子方程式为H++OH-═H2O,
故答案为:H++OH-═H2O;
(4)镁能在氮气中燃烧,生成氮化镁,氮化镁与水反应可产生一种使湿润红色石蕊试纸变蓝的气体为氨气,则氮化镁与盐酸反应的化学方程式为Mg3N2+8HCl=3MgCl2+2NH4Cl,
故答案为:Mg3N2+8HCl=3MgCl2+2NH4Cl.
点评 本题考查元素的推断以及元素化合物知识,注意把握原子的结构特点,结合元素周期律知识进行推断,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体也从下口放出 | |
| B. | 钠保存在煤油中 | |
| C. | 用洁净的铂丝蘸取某溶液在酒精灯火焰上灼烧时,火焰呈黄色,说明原溶液中含有Na+ | |
| D. | 可用CCl4萃取溴水中的溴单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠的制取:2NaCl(熔融)$\stackrel{通直流电}{→}$2Na+C12↑ | |
| B. | 金属镁的制取:MgO+CO$\stackrel{加热}{→}$Mg+CO2 | |
| C. | 金属铬的制取:Cr2O3+2Al$\stackrel{高温}{→}$2Cr+Al2O3 | |
| D. | 金属汞的制取:2HgO$\stackrel{加热}{→}$2Hg+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 向Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入NaOH体积V之间的关系如图所示.则混合溶液中Al2(SO4)3和MgSO4的物质的量之比为1:2.
向Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入NaOH体积V之间的关系如图所示.则混合溶液中Al2(SO4)3和MgSO4的物质的量之比为1:2.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
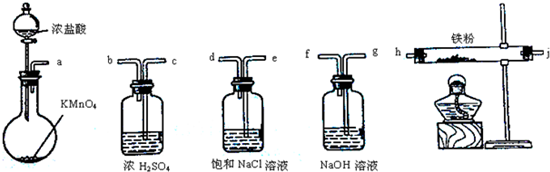
| A. | a-b-c-d-e-e-f-g-h | B. | a-e-d-c-b-h-j-g | ||
| C. | a-d-e-c-b-h-j-g | D. | a-c-b-d-e-h-j-f |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它只有一种氧化物Cs2O | B. | 它与水剧烈反应 | ||
| C. | Cs+具有很强的氧化性 | D. | CsHCO3受热不易分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com