
甲醇是重要的化工原料,在日常生活中有着广泛的应用。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
反应Ⅱ:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为_________________。
②对于反应Ⅰ,下图甲表示能量的变化;图乙表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时闻峦化。

在“图甲”中,曲线__________(填:“a”或“b”)表示使用了催化剂;该反应属于________(填:“吸热”、“放热”)反应。在图乙中从反应开始到建立平衡,用H2浓度变化表示的反应速率为_____________;该温度下CO(g)+2H2(g) CH3OH(g)的化学平衡常数为__________.
CH3OH(g)的化学平衡常数为__________.
③对于反应Ⅱ,在一定温度时,将lmol CO2年和3mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为a,则容器内的平衡压强与起始压强之比为__________;若容器容积不变,下列措施可增加甲醇产率的是____________。
a.升高温度
b.增加CO2的量
c.充入He,使体系总压强增大
d.按原比例再充入CO2和H2
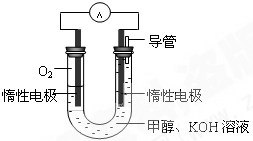
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种 污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程。

①阳极电极反应式为____________。
②除去甲醇的离子方程式为________________。
(14分)(1)①反应I符合“原子经济性”的原则即原子利用率为100%(1分)
②b(1分) 放热(1分) 0.15mol/(L·min)(2分) 12(1分)③1- (2分) bd(2分)
(2分) bd(2分)
(2)①CO2+-e-=CO3+(2分)
②6 CO3++CH3OH+H2O=CO2↑+6 CO2++6H+(2分)
【解析】
试题分析:(1)①根据反应I和反应Ⅱ的生成物可知,反应I中生成物只有一种,而反应Ⅱ中还有水生成,即反应I符合“原子经济性”的原则即原子利用率为100%,所以反应Ⅰ优于反应Ⅱ。
②根据图像甲可知,曲线b的活化能低于曲线a的活化能,所以曲线b表示使用了催化剂;同样根据图像甲可知,反应物的总能量高于生成物的总能量,所以反应是放热反应;根据图像乙可知,反应进行到10min是反应达到平衡状态,此时生成的甲醇浓度是0.75mol/L,则根据反应I可知,消耗氢气的浓度是1.5mol/L,所以氢气表示的反应速率是1.5mol/L÷10min=0.15mol/(L·min);平衡时氢气的浓度是2mol/L-1.5mol/L=0.5mol/L,所以根据CO和甲醇的平衡浓度可知,该温度下反应的平衡常数K= =12。
=12。
③
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始量(mol/L) 1 3 0 0
转化量(mol/L) a 3a a a
平衡量(mol/L) 1-a 3-3a a a
则根据压强之比是相应的物质的量之比可知
容器内的平衡压强与起始压强之比为 =1-
=1-
a.因正反应放热,升高温度可使平衡向逆反应方向移动,不能增加甲醇产率,故a不正确;
b.增加CO2的量,平衡向正反应方向移动,所以可以增加甲醇产率,故b正确;
c.充入He,使体系总压强增大,对于参加反应的物质来说,浓度不变,平衡不移动,甲醇产率不变,故c错误;
d.按原比例再充入CO2和H2压强增大,平衡向正反应方向移动,可以增加甲醇产率,故d正确。
答案选bd。
(2)①原电池中阳极失去电子,所以根据装置图可知,CO2+在阳极失去电子,阳极电极反应式为CO2+-e-=CO3+。
②Co3+做氧化剂,能把水中的甲醇氧化成CO2而净化,反应的离子方程式是6 CO3++CH3OH+H2O=CO2↑+6 CO2++6H+。
考点:考查绿色化学、反应热的判断、反应速率和平衡常数的计算、外界条件对平衡状态的影响、电解池的有关应用和电极反应式的书写


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
 甲醇是重要的化工原料,在日常生活中有着广泛的应用.
甲醇是重要的化工原料,在日常生活中有着广泛的应用. CH3OH(g)△H1
CH3OH(g)△H1 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源:2014届云南省昆明市高三上学期第一次摸底调研测试化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料和清洁液体燃料。工业上可利用CO或CO2来生产甲醇。甲醇制
备的相关信息如下表:

(1)反应②是____反应(选填“吸热”“放热”)。
(2)据上表信息推导出 、
、 与
与 之间的关系,
之间的关系, =______用
=______用 、
、 表示)。500℃时测得反应③在某时刻,
表示)。500℃时测得反应③在某时刻, 的浓度(mol/L)分别为0 8、0.1、0 3、0 15,此时
的浓度(mol/L)分别为0 8、0.1、0 3、0 15,此时 (选填“>”“<”“=”)。
(选填“>”“<”“=”)。
(3)若某温度下反应①从开始到平衡CO和CH3OH的浓度变化如图一所示,则用H2浓度变化表示此段时间内该反应的平均速.v(H2)=
若某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图二所示,则平衡状态由A变到B时,平衡常数 (选填“>”“<”“=”)。
(选填“>”“<”“=”)。

(4)一定温度下,在体积固定的密闭容器中发生反应②,可判断该反应已经达到平衡的是____。(用相应字母表示)
A.容器中总压强不变
B.混台气体的平均摩尔质量也始终保持不变,
C.混合气体的密度不变
D.CO2(g)或CO(g)的浓度不变
(5)一定条件下甲醇与一氧化碳反应可合成醋酸。室温下,将a mol/L醋酸溶液与bmol/LNaOH溶液等体积混合。若溶液显中性,则a_________b(选填“>”“<”“=”)。若c(Na+)<c(CH3COO-),则溶液显____性(选填“酸”“碱…中”)。
查看答案和解析>>
科目:高中化学 来源:宁夏自治区模拟题 题型:填空题
 CH3OH(g) △H1
CH3OH(g) △H1  CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2 

查看答案和解析>>
科目:高中化学 来源:2011年宁夏银川一中高考化学三模试卷(解析版) 题型:解答题
 CH3OH(g)△H1
CH3OH(g)△H1 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com