
(10��) )��Ԫ�����Ŷ���̬�������Ļ�������������������з�������Ҫ�����á�����������⣺
��1����һ�ܱ������У��������»�ѧ��Ӧ��
N2(g)+3H2(g) 2NH3(g) ��H��0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
2NH3(g) ��H��0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
| T | 298 K | 398 K | 498 K | �� |
| K | 4.1��106 | K1 | K2 | �� |
��1�� ��> ��1�֣� ��A��C��D��2�֣��� �ۼ�С ��1�֣��� ���䣨1��; �� > ��1�֣���
��2�� �� 2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ��H=��1225.6 kJ/mol ��2�֣�
�� N2H4��4e��=N2+4H+ ��2�֣�
���������������1�� �����ڸ÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����������¶ȣ�����ƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ������÷�Ӧ���淴Ӧ�����ƶ�������K1>K2����A��2v(H2)��=3v(NH3)���������ʵ�Ũ�Ȳ��䣬��Ӧ�ﵽƽ�⣬��ȷ��B��3v(N2)��=v(H2)�������ʵ�Ũ�Ȳ��䣬��Ӧ�ﵽƽ�⣬��������v(N2)��=3v(H2)�������ʵ�Ũ�ȷ����ı䣬��Ӧδ�ﵽƽ�⣬����C�����ڸ÷�Ӧ�Ƿ�Ӧǰ������������ȵķ�Ӧ��������������ѹǿ���ֲ��䣬��Ӧ�ﵽƽ�⣬��ȷ��D����Ϊ��Ӧǰ����������ʵ������ȣ����μӷ�Ӧ�����ʶ������壬�������䣬��������������ƽ��Ħ���������ֲ��䣬����������ʵ������䣬��Ӧ�ﵽƽ�⣬��ȷ������ά��������ѹǿ���䣬�ﵽƽ��״̬������������ͨ��һ������N2�����������ݻ��������ʵ�Ũ�ȼ�С�����Դ�ʱ�淴Ӧ���ʼ�С�������¶Ȳ��䣬����ƽ�ⳣ�����䣻����֪AgCl�����ڰ�ˮ�У���AgBr�����ڰ�ˮ�У�˵����ǰ�ߵ���Һ��Ag+��Ũ�ȴ���Ksp(AgCl) > Ksp(AgBr)��( 2 )�ٸ�������ɵø÷�Ӧ���Ȼ�ѧ����ʽ��2N2H4(l)+N2O4(l) =3N2(g)+ 4H2O(l) ��H=��1225.6 kJ/mol�������ڸ÷�Ӧ��������ԭ��Ӧ�����Կ�����Ƴ�ԭ��ء�ȼ��N2H4��ԭ��صĸ�����N2O4��ԭ��ص��������ϣ�������Ӧʽ��N2H4��4e��=N2+4H+ ��
���㣺���黯ѧƽ�ⳣ���ıȽϡ�ƽ��״̬���жϡ������ܽ�ȴ�С�ıȽϡ��Ȼ�ѧ����ʽ����д��ԭ��ط�Ӧԭ����Ӧ�õ�֪ʶ��


 ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ���¶��£����ݻ�Ϊ2L���ܱ�����ͨ���������������ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ���Ը÷�Ӧ���ƶϺ������ǣ� ��
A.�÷�Ӧ�Ļ�ѧ����ʽΪ3B+4D=6A+2C
B.��Ӧ���е�6sʱ��(B)=��(C)
C.��Ӧ���е�6sʱ����B��ʾ��ƽ����Ӧ����Ϊ0.05mol��L-1��s-1
D.��Ӧ���е�6sʱ����Ӧֹͣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���̶��ݻ����ܱ������г���2molNO2��һ���¶��½�������ƽ�⣺2NO2 N2O4����ʱƽ��������NO2���������Ϊx%�����ٳ���1mol N2O4�����¶Ȳ��������£��ﵽ�µ�ƽ��ʱ�����NO2���������Ϊy%����x��y�Ĵ�С��ϵ��ȷ���ǣ� ��
N2O4����ʱƽ��������NO2���������Ϊx%�����ٳ���1mol N2O4�����¶Ȳ��������£��ﵽ�µ�ƽ��ʱ�����NO2���������Ϊy%����x��y�Ĵ�С��ϵ��ȷ���ǣ� ��
| A��x>y | B��x<y | C��x=y | D������ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
2013��9��,�й��������е������������ص���������,����?�ӱ�?���ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ,�����ض���Ⱦ?����β��?ȼú����?����ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��?
��1������β����������Ҫԭ��Ϊ; , ��һ���¶���,��һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬?
, ��һ���¶���,��һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬?
�����жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�� ?
| A���ڵ�λʱ��������1molCO2��ͬʱ������lmolCO |
| B�����������ܶȲ��ٸı� |
| C����������ƽ����Է����������ٸı� |
| D����������ѹǿ���ٱ仯 |


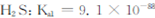 ;
; ?
? ;
;  ?)
?)  ,�ֽ���ͬ����CO(g)��H20(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ,�õ�������������:
,�ֽ���ͬ����CO(g)��H20(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ,�õ�������������: 
 0(�<����>��);
0(�<����>��); �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��6�֣�ÿ��2�֣���ͼ��ʾ������800��ʱ������A��B��C�����������ϵ�и�����Ũ����ʱ��仯���������ش�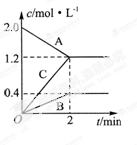
��1���÷�Ӧ�ķ�Ӧ���� ��
��2���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3�����ﵽƽ��״̬��ʱ��Ϊ2min����A���ʵ�ƽ����Ӧ����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(7��)��һ���ܱ������У���һ�����ҿɻ������壬���߷ֱ���п��淴Ӧ�������ʵ������£�M��N��PΪ2.5mol��3.0mol��1.0mol��A��C��D��Ϊ0.50mol��B�����ʵ���Ϊx����x�����ʵ�����һ����Χ�ڱ仯��������ͨ�����ڷ�Ӧ�����¶ȣ�ʹ���෴Ӧ���ﵽƽ�⣬�Ҹ����ڷ�Ӧ��������λ�á��ﵽƽ����M��ת����Ϊ75%����д�հף�
��1���ﵽƽ���Ӧ�����������ܵ����ʵ���Ϊ mol��
��2����Ҫʹ���ҷ�Ӧ��ʼʱV��>V����x��ȡֵ��Χ ��
��3����Ҫʹ���ҷ�Ӧ��ʼʱV��<V����x��ȡֵ��Χ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(10��)����ѡ����ʷ�������ĸ������գ�
�ٴӺ�ˮ����ȡ����________�� �� úת��Ϊ��̿��ú���͵�________��
�� ��ҵ������������ȡ������________�� �� �ᴿ������������________��
A�����ˡ�B���ѽ⡡C������D���ѻ���E������F����ԭ��
G����⡡H���ܽ⡡I��������J��������K������
��ij���淴Ӧ��0��2���ӽ��й����У� �ڲ�ͬ��Ӧʱ������ʵ����ı仯�������ͼ��ʾ����÷�Ӧ�ĵķ�Ӧ���� ���������� ���˷�Ӧ �����ǻ��ǣ����淴Ӧ����Ӧ��ʼ��2����ʱ�� _____ ���ܻ��ܣ���C��ʾ��Ӧ���ʣ�2���Ӻ�A��B��C�����ʵ���������ʱ��ı仯���仯��˵������������£���Ӧ�Ѵﵽ�� ____ ״̬����ʱ����Ӧ���� �淴Ӧ���ʣ�����ڻ��ڣ���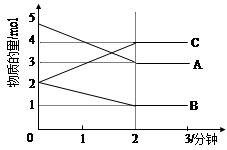
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����仯�����������������ϵ���С�
��1����ͼ��ʵ�����о���ˮ����բ��ͬ��λ��ʴ���������ʾ��ͼ��
�ٸõ绯��ʴ��Ϊ ��
��ͼ��A��B������Ƚϣ���ʴ�������� (����ĸ)��
��2��ʵ���Ҿ����õ�FeCl3��Һ��������FeCl3��Һʱ����������� �� ����FeCl3��Һ��̼��������Һ��ϣ����������ɫ��������ɫ���壬�÷�Ӧ�����ӷ���ʽΪ ��
��3����֪t��ʱ����ӦFeO(s)+CO(g) Fe( s) +CO2(g)��ƽ�ⳣ��K= 0.25��
Fe( s) +CO2(g)��ƽ�ⳣ��K= 0.25��
��t��ʱ����Ӧ�ﵽƽ��ʱn(CO2)��n(CO)=
������1L�ܱ������м���0.02 mol FeO(s)����ͨ��x mol CO��t��ʱ��Ӧ�ﵽƽ�⡣��ʱ
FeO(s)ת����Ϊ50%����x= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣�����KMnO4��Һ������ᣨH2C2O4����Һ��Ӧ��ij̽��С�����÷�Ӧ��������Һ��ɫ��ʧ�����ķ������о�Ӱ�췴Ӧ���ʵ����ء�
��.ʵ��ǰ������Ũ��Ϊ0.1000mol?L-1����KMnO4����Һ�ζ�δ֪Ũ�ȵIJ��ᡣ
��1��д���ζ������з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2���ζ������в����ζ��ܵ�ͼʾ��ȷ���� ��

��3�����ζ�ǰ�ζ��ܼ��촦�����ݣ��ζ�����ʧ����ʹ��õIJ�����ҺŨ�� ���ƫ�ߡ�����ƫ�͡������䡱����
��.ͨ���ζ�ʵ��õ�������Һ��Ũ��Ϊ0.2000mol��L-1 ���øò�����Һ���±����к���ʵ�飨ÿ��ʵ�������Һ��������Ϊ8mL����
��4��д������a ��Ӧ��ʵ��Ŀ�� ����50��Cʱ������Ũ��c(H2C2O4)�淴Ӧʱ��t�ı仯���� ����ͼ��ʾ�����������������䣬����ͼ�л���25��Cʱc(H2C2O4)��t�ı仯����ʾ��ͼ�� 
��5����С��ͬѧ��ʵ��1��3�ֱ����������ʵ�飬�������ʵ�����ݣ��ӻ�����ȿ�ʼ��ʱ����
�����������ݺ�ó���������������ͬʱ�����Ը��������Һ��Ũ��ԽС����ɫʱ���Խ�̣�����Ӧ���ʾ�Խ�족�Ľ��ۡ���ͬѧ��Ϊ��С�顰̽����Ӧ��Ũ�ȶ�����Ӱ�족��ʵ�鷽������д������⣬�Ӷ��õ��˴����ʵ����ۣ��������ͬѧ�Ľ���ʵ�鷽�� ______________________��
��6����ʵ����ʹ�õĴ���Ӧѡ��MnSO4����MnCl2��ԭ��������ӷ���ʽ��ʾΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com