





| A.①② | B.②④ | C.②③ | D.①④ |
科目:高中化学 来源:不详 题型:单选题
| A.铜与氯化亚铁常温下混和 | B.一氧化碳通过灼热的三氧化二铁 |
| C.氢气通过硫酸亚铁溶液 | D.铝和四氧化三铁混合加热至高温 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
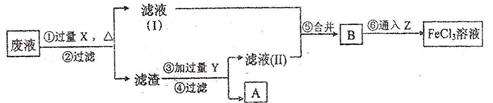
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.耐腐蚀性 | B.还原性 | C.热传导性 | D.延展性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

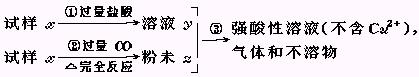
 (1)请写出步骤③中所发生的全部反应的离子方程式.
(1)请写出步骤③中所发生的全部反应的离子方程式. (2)若全部的溶液y和全部的粉末Z充分反应后,生成的不溶物的质量是m,则每份试样x中氧化铜的质量为 (用m表示).
(2)若全部的溶液y和全部的粉末Z充分反应后,生成的不溶物的质量是m,则每份试样x中氧化铜的质量为 (用m表示).查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入足量镁粉的Fe2(SO4)3溶液 |
| B.加入过量铁粉的稀硝酸溶液 |
| C.铁丝在足量的氯气中燃烧后,所得产物的溶液 |
| D.长期暴露在空气中的绿矾溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
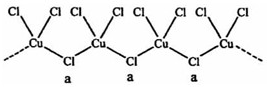
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com