
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A、A电极是负极 |
| B、外电路中电子由B电极通过导线流向A电极 |
| C、产物为无污染的水,属于环境友好电池 |
| D、该电池的总反应:2H2+O2═2H2O |


科目:高中化学 来源: 题型:
 )、甲酸甲酯(HCOOCH3).其中:
)、甲酸甲酯(HCOOCH3).其中:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将易腐败的食物储存在冰箱里 |
| B、将块状药品研细后再进行反应 |
| C、双氧水分解时加入二氧化锰 |
| D、用较浓的盐酸代替稀盐酸与锌反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾可除去水中的悬浮颗粒等杂质,所以可用作净水剂 |
| B、黄瓜含有丰富的维生素C,热锅爆炸能减少维生素C的流失 |
| C、石英玻璃纤维传导光的能力非常强,所以常用于光缆通信 |
| D、可用燃烧的方法鉴别羊毛围巾和合成纤维围巾 |
查看答案和解析>>
科目:高中化学 来源: 题型:
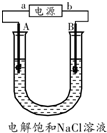 电解饱和食盐水是氯碱工业的基础.以下是实验室中电解饱和食盐水的装置图,A、B均为石墨电极,U形管内装有足量的饱和食盐水.通电几分钟后,将湿润的碘化钾淀粉试纸放在A电极一端的管口,试纸变蓝色.请回答:
电解饱和食盐水是氯碱工业的基础.以下是实验室中电解饱和食盐水的装置图,A、B均为石墨电极,U形管内装有足量的饱和食盐水.通电几分钟后,将湿润的碘化钾淀粉试纸放在A电极一端的管口,试纸变蓝色.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com