
”¾ĢāÄæ”æīŃŹĒŅ»ÖÖÖŲŅŖµÄ½šŹō£¬ŅŌīŃĢśæó[Ö÷ŅŖ³É·ÖĪŖīŃĖįŃĒĢś£ØFeTiO3£©£¬»¹ŗ¬ÓŠÉŁĮæFe2O3]ĪŖŌĮĻÖʱøīŃµÄ¹¤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾”£
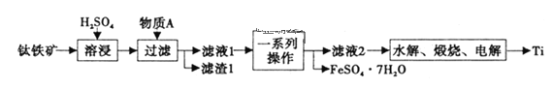
£Ø1£©ĀĖŅŗ1ÖŠīŃŌŖĖŲŅŌTiO2+ŠĪŹ½“ęŌŚ£¬Ōņ”°Čܽž”±¹ż³Ģ·¢ÉśµÄÖ÷ŅŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___”£
£Ø2£©ĪļÖŹAĪŖ___£ØĢī»ÆѧŹ½£©£¬”°Ņ»ĻµĮŠ²Ł×÷”±ĪŖ___”£
£Ø3£©”°Ė®½ā”±²½ÖčÖŠÉś³ÉTiO2”¤xH2O£¬ĪŖĢįøßTiO2”¤xH2OµÄ²śĀŹ£¬æɲÉČ”µÄ“ėŹ©ÓŠ___”¢___”££ØŠ“³öĮ½Ģõ£©”£
£Ø4£©½«ÉŁĮæFeSO4”¤7H2OČÜÓŚĖ®£¬¼ÓČėŅ»¶ØĮæµÄNaHCO3ČÜŅŗ£¬æÉÖʵĆFeCO3£¬Š“³ö·“Ó¦µÄĄė×Ó·½³ĢŹ½___£»Čō·“Ó¦ŗóµÄČÜŅŗÖŠc£ØFe2+£©=2”Į10-6mol”¤L-1£¬ŌņČÜŅŗÖŠc£ØCO32-£©=___mol”¤L-1”££ØŅŃÖŖ£ŗKSP£ØFeCO3£©=2.025”Į10-11£©
”¾“š°ø”æFeTiO3£«2H2SO4![]() TiOSO4£«FeSO4£«2H2O Fe Õō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢¹żĀĖ ¼ÓĖ®Ļ”ŹĶ·“Ó¦Īļ ¼Ó¼īÖŠŗĶÉś³ÉµÄĖį”¢¼ÓČČµČ Fe2++2HCO3-=FeCO3”ż+CO2”ü+H2O 1”Į10-5
TiOSO4£«FeSO4£«2H2O Fe Õō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢¹żĀĖ ¼ÓĖ®Ļ”ŹĶ·“Ó¦Īļ ¼Ó¼īÖŠŗĶÉś³ÉµÄĖį”¢¼ÓČČµČ Fe2++2HCO3-=FeCO3”ż+CO2”ü+H2O 1”Į10-5
”¾½āĪö”æ
īŃĢśæóÓėĮņĖį·“Ӧɜ³ÉĮņĖįīŃŗĶĮņĖįŃĒĢś£¬Ńõ»ÆĢśÓėĮņĖį·“Ӧɜ³ÉĮņĖįĢśŗĶĖ®£¬ČÜŅŗÖŠŗ¬ÓŠŃĒĢśĄė×Ó”¢ĢśĄė×ÓŗĶTiO2+£¬øł¾ŻĮ÷³ĢĶ¼æÉÖŖ£¬Ņ»ĻµĮŠ²Ł×÷ŗóÖĘČ”ĮņĖįŃĒĢś¾§Ģ壬ŌņĪļÖŹAĪŖFe£¬ÓėČÜŅŗÖŠµÄĢśĄė×Ó·“Ó¦£¬Éś³ÉŃĒĢśĄė×Ó£»ĮņĖįŃĒĢś¾¹żÕō·¢ÅØĖõ”¢½µĪĀ½į¾§µĆµ½ĮņĖįŃĒĢś¾§Ģ壻TiO2+Ąė×Ó¾¹żĖ®½āÉś³ÉTiO2”¤xH2O£¬ŌŁ¾¹żģŃÉÕ”¢µē½āÖĘČ”Ti”£
£Ø1£©¾¹żĮ÷³ĢæÉÖŖ£¬ČܽžŹ±µÄÖ÷ŅŖ·“Ó¦ĪŖīŃĢśæóÓėĮņĖį·“Ӧɜ³ÉTiO2+”¢Fe2+”¢H2O£¬·“Ó¦µÄ·½³ĢŹ½ĪŖFeTiO3£«2H2SO4![]() TiOSO4£«FeSO4£«2H2O£»
TiOSO4£«FeSO4£«2H2O£»
£Ø2£©īŃĢśæóÖŠŗ¬ÓŠÉŁĮæµÄŃõ»ÆĢśÓėĮņĖį·“ӦɜĮņĖįĢśŗĶĖ®£¬·“Ó¦²śĪļÓŠĮņĖįŃĒĢś¾§Ģ壬ŌņŠčŅŖ³żČ„ČÜŅŗÖŠµÄĢśĄė×Ó£¬ĒŅ²»ŅżČėŠĀµÄŌÓÖŹ£¬ŌņĪļÖŹAĪŖĢś·Ū£»ÖĘČ”µÄĪŖĮņĖįŃĒĢś¾§Ģ壬Ņ»ĻµĮŠ²Ł×÷ĪŖÕō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢¹żĀĖ¼“æÉÖĘČ”ĮņĖįŃĒĢś¾§Ģ壻
£Ø3£©ČÜŅŗÖŠµÄTiO2+Ė®½ā·“Ó¦Ź½ĪŖTiO2++£Øx+1£©H2O=TiO2”¤xH2O+2H+£¬ĪŖĢįøßTiO2”¤xH2OµÄ²śĀŹ£¬æÉŅŌ¼ÓĖ®Ļ”ŹĶ»ņ¼ÓČė¼ī”¢¼ÓČČµČ£¬Ź¹Ę½ŗāÕżĻņŅĘ¶Æ£»
£Ø4£©FeSO4ĪŖĒæĖįČõ¼īŃĪ£¬ČÜŅŗĻŌĖįŠŌ£¬NaHCO3ĪŖĒæ¼īČõĖįŃĪ£¬ČÜŅŗĻŌ¼īŠŌ£¬Į½ČÜŅŗ»ģŗĻŹ±£¬Ļą»„“Ł½ųĖ®½āæÉÉś³ÉĢ¼ĖįŃĒĢś”¢¶žŃõ»ÆĢ¼ŗĶĖ®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖFe2++2HCO3-=FeCO3”ż+CO2”ü+H2O£»KSP£ØFeCO3£©= c£ØFe2+£©”Įc£ØCO32-£©£¬Ōņc£ØCO32-£©= KSP£ØFeCO3£©/ c£ØFe2+£©=2.025”Į10-11/2”Į10-6=1.0125”Į10-5 mol”¤L-1”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČā¹šĖį(M)ŹĒŅ½Ņ©”¢ĻćĮĻµÄÖŠ¼äĢ壬ŹµŃéŹŅÓÉ·¼Ļć»ÆŗĻĪļAÖʱøMµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
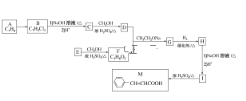
ŅŃÖŖ£ŗ¢Ł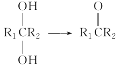 (R1”¢R2±ķŹ¾ĒāŌ×Ó»ņĢž»ł)
(R1”¢R2±ķŹ¾ĒāŌ×Ó»ņĢž»ł)
¢ŚR1COOR2£«R3CH2COOR4![]()
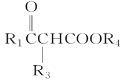 £«R2OH
£«R2OH
(R1”¢R3±ķŹ¾ĒāŌ×Ó»ņĢž»ł£¬R2”¢R4±ķŹ¾Ģž»ł)
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ(1)A”śBµÄĢõ¼žĪŖ________”£
(2)EÖŠĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘĪŖ________”£
(3)HµÄ½į¹¹¼ņŹ½ĪŖ________”£(4)I”śMµÄ·“Ó¦ĄąŠĶĪŖ________”£
(5)D£«F”śGµÄ»Æѧ·½³ĢŹ½ĪŖ________________________”£
(6)Ķ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄIµÄĶ¬·ÖŅģ¹¹ĢåÓŠ________ÖÖ(²»æ¼ĀĒĮ¢ĢåŅģ¹¹)£¬ČĪŠ“Ņ»ÖÖŗĖ“Ź²ÕńĒāĘ×ÖŠÓŠ6×éĪüŹÕ·åĒŅ·åĆ껿֮±ČĪŖ1£ŗ2£ŗ2£ŗ2£ŗ2£ŗ1µÄ½į¹¹¼ņŹ½ĪŖ_______”£
¢ŁÄÜ·¢ÉśĻŌÉ«·“Ó¦ŗĶŅų¾µ·“Ó¦””¢Ś±½»·ÉĻĮ¬ÓŠĮ½øöČ”“ś»ł
(7)²ĪÕÕÉĻŹö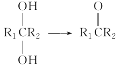 ŠÅĻ¢£¬ŅŌ¼×ĶéŗĶ±½·ÓĪŖŌĮĻ(ĘäĖūĪŽ»śŹŌ¼ĮČĪŃ”)£¬Éč¼ĘÖʱø
ŠÅĻ¢£¬ŅŌ¼×ĶéŗĶ±½·ÓĪŖŌĮĻ(ĘäĖūĪŽ»śŹŌ¼ĮČĪŃ”)£¬Éč¼ĘÖʱø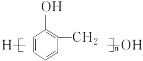 µÄŗĻ³ÉĀ·Ļß_______________________”£
µÄŗĻ³ÉĀ·Ļß_______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓĆĆܶČĪŖ1.25 g/mL”¢ÖŹĮæ·ÖŹżĪŖ36.5%µÄÅØŃĪĖįÅäÖĘ240 mL 0.1 mol/LµÄŃĪĖį£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ÅØŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ_________”£
(2)ÅäÖĘ 240 mL 0.1mol/LµÄŃĪĖį”£
Ó¦ĮæČ”ÅØŃĪĖįĢå»ż/mL | ӦєÓĆČŻĮæĘæµÄ¹ęøń/mL |
______ | ______ |
(3)ÅäÖĘŹ±£¬ĘäÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ(×ÖÄø±ķŹ¾£¬Ćæøö×ÖÄøÖ»ÄÜÓĆŅ»“Ī )_________
A. ÓĆ30 mLĖ®Ļ“µÓÉÕ±ÄŚ±ŚŗĶ²£Į§°ō23“Ī£¬Ļ“µÓŅŗ¾ł×¢ČėČŻĮæĘ棬Õńµ“
B. ÓĆĮæĶ²»“Č·ĮæČ”ĖłŠčµÄÅØŃĪĖįµÄĢå»ż£¬µ¹ČėÉÕ±ÖŠ£¬ŌŁ¼ÓČėÉŁĮæĖ®(Ō¼30 mL)£¬ÓĆ²£Į§°ōĀżĀż½Į¶Æ£¬Ź¹Ęä»ģŗĻ¾łŌČ
C. ½«ŅŃĄäČ“µÄŃĪĖįŃŲ²£Į§°ō×¢ČėČŻĮæĘæÖŠ
D. ½«ČŻĮæĘæøĒ½ō£¬Õńµ“£¬Ņ”ŌČ
E. øÄÓĆ½ŗĶ·µĪ¹Ü¼ÓĖ®£¬Ź¹ČÜŅŗ°¼ŅŗĆęĒ”ŗĆÓėæĢ¶ČĻßĻąĒŠ
F. ¼ĢŠųĶłČŻĮæĘæÄŚŠ”ŠÄ¼ÓĖ®£¬Ö±µ½ŅŗĆę½Ó½üæĢ¶ČĻß12 cm“¦
(4)ČōŹµŃéÖŠÓöµ½ĻĀĮŠĒéæö£¬¶ŌŃĪĖįČÜŅŗµÄĪļÖŹµÄĮæÅضČÓŠŗĪÓ°Ļģ(Ģī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°²»±ä”±)?
¢ŁÓĆÓŚĻ”ŹĶŃĪĖįµÄÉÕ±Ī“Ļ“µÓ_________”£
¢ŚČŻĮæĘæÖŠŌÓŠÉŁĮæÕōĮóĖ®_________”£
¢Ū¶ØČŻŹ±¹Ū²ģŅŗĆęø©ŹÓ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ273KŗĶ101kPaµÄĢõ¼žĻĀ,½«2.00gŗ¤Ęų,1.40gµŖĘųŗĶ1.60gŃõĘų»ģŗĻ,Ēó£ŗ
(1)øĆ»ģŗĻĘųĢåµÄ×ÜĪļÖŹµÄĮæĪŖ______________
(2)øĆ»ģŗĻĘųĢåµÄĢå»żŹĒ_______________
(3)øĆ»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæĪŖ_________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒ²æ·Ö¶ĢÖÜĘŚŌŖĖŲŌ×Ó°ė¾¶ÓėŌ×ÓŠņŹżµÄ¹ŲĻµĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
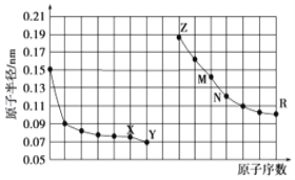
A.MµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÄÜ·Ö±šÓėZ”¢RµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·“Ó¦
B.æÉÓĆ»¹Ō¼Į»¹ŌRµÄ¼ņµ„Ąė×ÓÖʱøRµ„ÖŹ
C.X”¢NĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļČŪµćŗܵĶ
D.¼ņµ„Ąė×ӵİė¾¶£ŗZ£¼X£¼Y
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖŹŅĪĀĻĀČܶȻż³£Źż£ŗKsp[Pb£ØOH£©2]=2”Į10-15£¬Ksp[Fe£ØOH£©2]=8”Į10-15”£µ±ČÜŅŗÖŠ½šŹōĄė×ÓÅØ¶ČŠ”ÓŚ10-5molL-1ŹÓĪŖ³ĮµķĶźČ«”£Ļņ20mLŗ¬0.10molL-1Pb2+ŗĶ0.10molL-1Fe2+µÄ»ģŗĻČÜŅŗÖŠµĪ¼Ó0.10molL-1NaOHČÜŅŗ£¬½šŹōŃōĄė×ÓÅضČÓėµĪČėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A.ĒśĻßA±ķŹ¾c(Pb2+)µÄĒśĻß
B.µ±ČÜŅŗpH=8Ź±£¬Fe2+æŖŹ¼³Įµķ£¬Pb2+³ĮµķĶźČ«
C.µĪČėNaOHČÜŅŗĢå»ż“óÓŚ30mLŹ±£¬ČÜŅŗÖŠc(Fe2+)=4c(Pb2+)
D.ŹŅĪĀĻĀ£¬µĪ¼ÓNaOHČÜŅŗ¹ż³ĢÖŠ£¬ ±ČÖµ²»¶ĻŌö“ó
±ČÖµ²»¶ĻŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķ±ź³öµÄŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·ÖŌŖĖŲ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
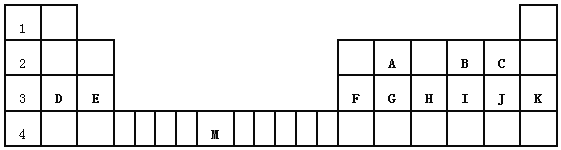
£Ø1£©³żĻ”ÓŠĘųĢåĶāµŚČżÖÜĘŚÖŠŌ×Ó°ė¾¶×īŠ”µÄŹĒ_____£ØĢīŌŖĖŲ·ūŗÅ£©
£Ø2£©±ķÖŠÓĆ×ÖÄø±ź³öµÄ12ÖÖŌŖĖŲÖŠ£¬»ÆѧŠŌÖŹ×ī²»»īĘƵďĒ_____£ØÓĆŌŖĖŲ·ūŗűķŹ¾£¬ĻĀĶ¬£©£¬½šŹōŠŌ×īĒæµÄŹĒ___£ØÓĆŌŖĖŲ·ūŗűķŹ¾£©£¬ŹōÓŚ¹ż¶ÉŌŖĖŲµÄŹĒ___£ØøĆæÕøńÓƱķÖŠµÄ×ÖÄø±ķŹ¾£©
£Ø3£©ŌŖĖŲBµÄµ„ÖŹŗ¬ÓŠµÄ»Æѧ¼üĪŖ_____”££ØĢī”°Ąė×Ó¼ü”ƔƔ¢”°¼«ŠŌ¹²¼Ū¼ü”±”¢”°·Ē¼«ŠŌ¹²¼Ū¼ü”±£©
£Ø4£©D”¢FŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________
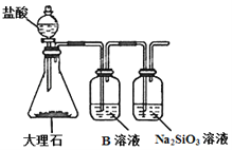
£Ø5£©ĪŖ±Č½ĻŌŖĖŲAŗĶGµÄ·Ē½šŹōŠŌĒæČõ£¬ÓĆĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé£Ø¼Š³ÖŅĒĘ÷ŅŃĀŌČ„£¬×°ÖĆĘųĆÜŠŌĮ¼ŗĆ£©”£ČÜŅŗBÓ¦øĆŃ”ÓĆ_____ČÜŅŗ£¬×÷ÓĆŹĒ_________£¬ÄÜĖµĆ÷AŗĶG·Ē½šŹōŠŌĒæČõµÄ»Æѧ·½³ĢŹ½ŹĒ£ŗ________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņVmL0.1mol/L°±Ė®ÖŠµĪ¼ÓµČĪļÖŹµÄĮæÅØ¶ČµÄĻ”H2SO4£¬²āµĆ»ģŗĻČÜŅŗµÄĪĀ¶ČŗĶpOH[pOH£½£lgc(OH£)]Ėę׿ÓČėĻ”ĮņĖįµÄĢå»żµÄ±ä»ÆČēĶ¼ĖłŹ¾(ŹµĻßĪŖĪĀ¶Č±ä»Æ£¬ŠéĻßĪŖpOH±ä»Æ)£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
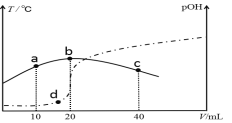
A. a”¢b”¢cČżµćÓÉĖ®µēĄėµÄc(H+)ŅĄ“Ī¼õŠ”
B. V£½40
C. bµćŹ±ČÜŅŗµÄpOH>pH
D. a”¢b”¢dČżµć¶ŌÓ¦NH3”¤H2OµÄµēĄė³£Źż£ŗK(b)>K(d)>K(a)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫 1molCOŗĶ 2molH2³äČėŅ»ČŻ»żĪŖ 1LµÄĆܱÕČŻĘ÷ÖŠ£¬·Ö±šŌŚ250”ćC”¢T”ćCĻĀ·¢Éś·“Ó¦£ŗCO(g)+2H2(g) ![]() CH3OH(g)”£øł¾ŻĶ¼£¬ĻĀĮŠ·ÖĪöÖŠÕżČ·µÄŹĒ£Ø £©
CH3OH(g)”£øł¾ŻĶ¼£¬ĻĀĮŠ·ÖĪöÖŠÕżČ·µÄŹĒ£Ø £©
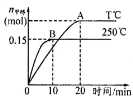
A. 250”ćCŹ±£¬·“Ó¦ŌŚĒ°10sµÄĘ½¾łĖŁĀŹ¦Ō(H2)=0.015mol/(L”¤min)
B. Ę½ŗāŹ±COµÄ×Ŗ»ÆĀŹ£ŗ250”ćC£¾T”ćC
C. ·“Ó¦“ļĘ½ŗāŗó£¬ĘäĖūĢõ¼ž²»±ä£¬Čō¼õŠ”ČŻ»żĢå»ż£¬CO Ģå»ż·ÖŹżŌö“ó
D. øĆ·“Ó¦µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com