
ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A£®1 mol N2Ėłŗ¬ÓŠµÄŌ×ÓŹżĪŖNA
B£®±ź×¼×“æöĻĀ£¬22.4 LĖ®ÖŠŗ¬ÓŠµÄĖ®·Ö×ÓŹżĪŖNA
C£®±ź×¼×“æöĻĀ£¬22.4 LĀČ»ÆĒāĖłŗ¬µÄŌ×ÓŹżĪŖNA
D£®24 g O2·Ö×ÓŗĶ24 g O3·Ö×ÓĖłŗ¬µÄŃõŌ×ÓŹżÄæĻąµČ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½ā¾«Į¶ĶŹ±£¬µ±Ņõ¼«Īö³ö32gĶŹ±£¬×ŖŅʵē×ÓŹżŠ”ÓŚNA | |
| B£® | ³£ĪĀĻĀ£¬1.0L 1.0 mol/LNaAlO2ČÜŅŗÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2NA | |
| C£® | µČĪļÖŹµÄĮæµÄøɱłŗĶĘĻĢŃĢĒÖŠĖłŗ¬Ģ¼Ō×ÓŹżÖ®±ČĪŖ1£ŗ6£¬ŃõŌ×ÓŹżÖ®±ČĪŖ1£ŗ3 | |
| D£® | 0.10 mol Fe·ŪÓė×ćĮæĖ®ÕōĘų·“Ӧɜ³ÉµÄH2·Ö×ÓŹżĪŖ0.10NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | m=8.7 g | |
| B£® | ·“Ó¦¹ż³ĢÖŠ×ŖŅʵē×Ó×ÜŹżĪŖ0.1 NA | |
| C£® | ·“Ó¦¹ż³ĢÖŠĘšŃõ»ÆŠŌ×÷ÓƵÄn£ØHCl£©=0.2mol | |
| D£® | ĀĖŅŗÖŠŃĪĖįµÄÅضČĪŖ$\frac{2}{3}$ mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”øßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻÖÓŠCO”¢CO2”¢O3£Ø³ōŃõ£©ČżÖÖĘųĢ壬ĖüĆĒ·Ö±š¶¼ŗ¬ÓŠ1 molŃõŌ×Ó£¬ŌņČżÖÖĘųĢåµÄĪļÖŹµÄĮæÖ®±ČĪŖ£Ø £©
A£®1£ŗ1£ŗ1 B£®1£ŗ2£ŗ3 C£®3£ŗ2£ŗ1 D£®6£ŗ3£ŗ2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĮ×ĖįøĘĢÕ“ÉÖĘŌģČĖĢå¹Ē÷Ą£¬ĄūÓƵďĒøĆ²ÄĮĻµÄÄĶøßĪĀ¹¦ÄÜ | |
| B£® | °±Ęų¾ßÓŠŃõ»ÆŠŌ£¬ÓĆÅØ°±Ė®¼ģŃéĀČĘų¹ÜµĄŹĒ·ńŠ¹Ā© | |
| C£® | Ģ¼ĖįÄĘČÜŅŗĻŌ¼īŠŌ£¬æÉÓĆČȵı„ŗĶĢ¼ĖįÄĘČÜŅŗ³żČ„½šŹō±ķĆęµÄÓĶĪŪ | |
| D£® | ¹¤ŅµÉś²ś²£Į§”¢Ė®Äą”¢ĢՓɶ¼ŅŖŹ¹ÓĆŹÆ»ŅŹÆ×öŌĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ1mol•L-1 | |
| B£® | ÅäÖĆøĆČÜŅŗŠčÓĆMgCl29.5g | |
| C£® | øĆČÜŅŗÓė200mL1mol•L-1NaClČÜŅŗµÄCl-µÄĪļÖŹµÄĮæÅضČĻąĶ¬ | |
| D£® | Č”10mLøĆČÜŅŗŌŁĻ”ÖĮ100mL£¬ĖłµĆČÜŅŗµÄCl-µÄĪļÖŹµÄĮæĪŖ0.02mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuSO4 | B£® | FeSO4•7H2O | C£® | KAl£ØSO4£©2•7H2O | D£® | Fe2£ØSO4£©3•7H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”ø߶žÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ijŹµŃ銔×éÓĆ0.50 mol/L NaOHČÜŅŗŗĶ0.50 mol/LĮņĖįČÜŅŗ½ųŠŠÖŠŗĶČČµÄ²ā¶Ø”£
¢ń£®ÅäÖĘ0.50 mol/L NaOHČÜŅŗ
£Ø1£©ČōŹµŃéÖŠ“óŌ¼ŅŖŹ¹ÓĆ245 mL NaOHČÜŅŗ£¬ÖĮÉŁŠčŅŖ³ĘĮæNaOH¹ĢĢå g”£
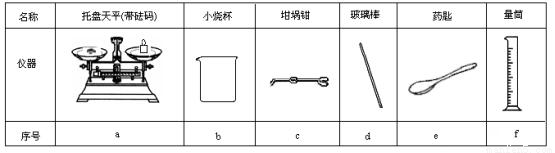
£Ø2£©“ÓĶ¼6ÖŠŃ”Ōń³ĘĮæNaOH¹ĢĢåĖłŠčŅŖµÄŅĒĘ÷ŹĒ£ØĢī×ÖÄø£©£ŗ ”£
¢ņ£®²ā¶ØÖŠŗĶČȵďµŃé×°ÖĆČēĶ¼7ĖłŹ¾”£

£Ø1£©Š“³öĻ”ĮņĖįŗĶĻ”ĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦±ķŹ¾ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½ £ØÖŠŗĶČČŹżÖµĪŖ57.3 kJ/mol£©£ŗ
£Ø2£©Č”50 mL NaOHČÜŅŗŗĶ30 mLĮņĖįČÜŅŗ½ųŠŠŹµŃ飬ŹµŃ鏿¾ŻČēĻĀ±ķ”£
¢ŁĒėĢīŠ“ĻĀ±ķÖŠµÄæÕ°×£ŗ
ŹµŃé“ĪŹż | ĘšŹ¼ĪĀ¶Čt1/”ę | ÖÕÖ¹ĪĀ¶Č t2/”ę[ | ĪĀ¶Č²īĘ½¾łÖµ £Øt2-t1£©/”ę | ||
H2SO4 | NaOH | Ę½¾łÖµ | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
¢Ś½üĖĘČĻĪŖ0.50 mol/L NaOHČÜŅŗŗĶ0.50 mol/LĮņĖįČÜŅŗµÄĆܶȶ¼ŹĒ1 g/cm3£¬ÖŠŗĶŗóÉś³ÉČÜŅŗµÄ±ČČČČŻc=4.18 J/(g”¤”ę)”£ŌņÖŠŗĶČČ”÷H= £ØČ”Š”ŹżµćŗóŅ»Ī»£©”£
¢ŪÉĻŹöŹµŃ鏿ֵ½į¹ūÓė57.3 kJ/molÓŠĘ«²ī£¬²śÉśĘ«²īµÄŌŅņæÉÄÜŹĒ£ØĢī×ÖÄø£© ”£
a£®ŹµŃé×°ÖƱ£ĪĀ”¢øōČČŠ§¹ū²ī
b£®ĮæČ”NaOHČÜŅŗµÄĢå»żŹ±ŃöŹÓ¶ĮŹż
c£®·Ö¶ą“Ī°ŃNaOHČÜŅŗµ¹ČėŹ¢ÓŠĮņĖįµÄŠ”ÉÕ±ÖŠ
d£®ÓĆĪĀ¶Č¼Ę²ā¶ØNaOHČÜŅŗĘšŹ¼ĪĀ¶ČŗóÖ±½Ó²ā¶ØH2SO4ČÜŅŗµÄĪĀ¶Č
£Ø3£©ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó³ĘĪŖ»ī»Æ·Ö×Ó£¬Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ/mol±ķŹ¾”£ĒėČĻÕę¹Ū²ģÓŅĶ¼£¬Č»ŗó»Ų“šĪŹĢā”£

¢ŁĶ¼ÖŠĖłŹ¾·“Ó¦ŹĒ_________£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦£¬øĆ·“Ó¦µÄ”÷H£½____________£ØÓĆŗ¬E1”¢E2µÄ“śŹżŹ½±ķŹ¾£©”£
¢Ś¶ŌÓŚĶ¬Ņ»·“Ó¦£¬Ķ¼ÖŠŠéĻߣآņ£©ÓėŹµĻߣآń£©Ļą±Č£¬»ī»ÆÄÜ“ó“ó½µµĶ£¬»ī»Æ·Ö×ӵİŁ·ÖŹżŌö¶ą£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬ÄćČĻĪŖ×īæÉÄܵÄŌŅņŹĒ_________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com