
| A. | ①②③⑤ | B. | ①②④⑤ | C. | ①③④ | D. | ①②③④ |
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:2017届内蒙古高三上月考二化学试卷(解析版) 题型:选择题
在如图的实验装置中,实验开始一段时间后,对看到的现象叙述不正确的是

A.苹果块会干瘪 B.胆矾晶体表面有“白斑”
C.小试管内有晶体析出 D.pH试纸变红
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟二化学试卷(解析版) 题型:实验题
某强酸性溶液X中可能含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是 .能证明该阴离子是否存在的简单实验操作为____ __.
(2)用离子方程表达下列反应:
①中生成气体A: .②中生成溶液H: .
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0ml时开始产生沉淀,55ml时沉淀的量达到最大值0.03mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025mol且保持不变,则原溶液中c(Fe2+)为 mol/L、c(Fe3+)为 mol/L、c(Cl﹣)为 mol/L.(若有些离子不存在,请填0mol/L)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.2 mol/(L•s) | B. | v(B)=0.6 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(D)=1 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B. | C. | D. |
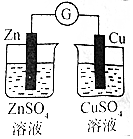 |  |  |  |
| 验证化学能转化为电能 | 验证氧化性:Cl2>Br2>I2 | 验证温度对平衡移动的影响 | 制取MgCl2固体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通式相同的两种有机物,其实验式也相同 | |
| B. | 等质量且通式相同的两种有机物完全燃烧耗氧量未必相同 | |
| C. | 通式相同的两种有机物要么互为同系物要么互为同分异构 | |
| D. | 实验式相同的两种有机物要么互为同系物要么互为同分异构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质氧化性:I2>Br2>Cl2 | B. | 碱性强弱:KOH>NaOH>Mg(OH)2 | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 热稳定性:PH3>H2S>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、SO42-、HCO3- | B. | Fe2+、K+、SO42-、NO3- | ||
| C. | Ba2+、K+、Cl-、NO3- | D. | Fe3+、K+、SCN-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池的负极反应为:2H++2e-=H2 | B. | 反应中Zn作氧化剂 | ||
| C. | 原电池的负极反应为:Zn-2e-=Zn2+ | D. | 反应中H2SO4作还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com