
标准状况下,一体积水能溶解700体积氨气,得到密度为0.9g/mL的氨水,计算此氨水的物质的量浓度为 。
科目:高中化学 来源: 题型:填空题
(10分)
(1)质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是 。
(2)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是_______。(填序号)
①NaAlO2 ② Ca(OH)2 ③Na2CO3 ④Al(OH)3
(3)氯水中含有多种成分。将紫色石蕊试液滴入氯水中,溶液显红色起作用的成分是
;过一会儿,溶液颜色逐渐褪去,起作用的成分是 ;
(4)标准状况下把11.2L氯气通入500ml0.8mol/LFeBr2溶液中,写出反应完全后的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
请完成下列填空:
(1)当SO2和SO3中分子个数比为1∶1 时,原子总数之比为 ,质量之比为 。
(2)中和含0.2 mol HCl的稀盐酸,需NaOH的质量为 g。
(3)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1,则:
①该气体的物质的量为 mol。
②该气体在标准状况下的体积为 L。
③该气体溶于水后形成V L溶液(不考虑反应),其溶液的物质的量浓度为 mol/L。
(4)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是 mol/L。
(5)用等体积的0.1mol/L的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO42-恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
过氧乙酸是一种弱酸性氧化剂,广泛用作漂白剂和高效杀菌消毒剂等。
Ⅰ、制备:冰醋酸与H2O2浓溶液按体积比1:1混合,加入适量浓硫酸,控制温度5℃~30℃,搅拌30min并静置4~6h。
反应原理为:H2O2+CH3COOH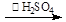
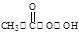 (过氧乙酸)+H2O
(过氧乙酸)+H2O
Ⅱ、含量测定:称取5.0000g过氧乙酸试样(液体),稀释至100mL备用。取上述稀释后过氧乙酸试样5.00mL,用0.0100 mol·L-1KMnO4溶液滴定到终点以除去其中的H2O2,随即加入10%KI溶液10mL,加入0.5%淀粉溶液3滴,摇匀,并用0.0500 mol·L-1Na2S2O3标准溶液滴定到蓝色刚好褪去(离子反应方程式为:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3标准溶液的总体积为20.00mL。
(1)制备过氧乙酸时,温度不宜过高,其原因可能是 。
(2)稀释样品时,除用到容量瓶及烧杯外,还用到的玻璃仪器有 、 。
(3)过氧乙酸溶液与KI反应的离子方程式为 。
(4)通过计算确定原试样中过氧乙酸的质量分数(写出计算过程)。 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有25℃101KPa条件下的氯化氢(HCl)气体49L(注:25℃101KPa条件下气体摩
尔体积为24.5L/mol)则:
①该气体所含原子总数为________________个。
②该气体的质量为_____________g。
③该气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为______________。④取出20.0 mL该溶液,配成浓度为2.00 mol/L的稀溶液,则稀释后溶液的体积是_________ ml。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某草酸盐晶体KxFey(C2O4)z?wH2O中铁为+3价,草酸根为-2价,且知x+y+z=7。取该晶体做了以下实验:
① 取4.910g晶体在不同温度下加热至恒重,所得固体的化学式和质量如下表:
| | 120℃ | 300℃ | 480℃ |
| 化学式 | KxFey(C2O4)z | KxFeyO(C2O4)z-1 | KxFeyO2(C2O4)z-2 |
| 质量 | 4.370g | 3.650g | 2.930 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)0.5 mol H2O的质量为_______________,其中含有_______________个水分子,共有_______________个原子。
(2)质量都是50g的HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是_______________;在相同温度和相同压强条件下,体积最大的是_______________,体积最小的是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
将50.0g含有NH4NO3、(NH4)2SO4及其它难溶物的混合物样品,溶于水,过滤后加入足量浓NaOH溶液共热,在标准状况下收集到13.44 L氨气,再向溶液中加入足量BaCl2溶液,产生沉淀46.6g,试计算混合物中NH4NO3的物质的量及(NH4)2SO4的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
向100 mL水中投入K和Al共15 g,充分反应后,剩余金属为1.8 g
(1)计算放出H2多少升(标准状况下)
(2)过滤出未反应的金属,向滤液中逐滴加入4 mol/L 的 H2SO4 溶液,生成沉淀的最大值是多少,此时消耗 H2SO4 溶液的体积是多少?
(3)生成沉淀后,再加入H2SO4 溶液,使沉淀刚好完全溶解,此时消耗 H2SO4 溶液的体积是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com