
【题目】过氧化氢和臭氧是用途很广的氧化剂。试回答下列问题:
(1)过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化KI的离子反应方程式:__________________________。
(2)Na2O2 、K2O2、 以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是_______(写电子式)。
(3).已知3.6 g碳在6.4 g氧气中燃烧,至反应物耗尽,测得放出热量a kJ。又知道12.0 g碳完全燃烧,放出热量为b kJ。则热化学方程式C(s)+![]() O2(g)===CO(g) ΔH=w,
O2(g)===CO(g) ΔH=w,
w等于 _____________
臭氧(O3)可以使湿润的淀粉-碘化钾试纸变蓝,反应的化学方程式为:
KI+O3+H2O→KOH+I2+O2(未配平) 回答问题:
①还原产物的化学式为 _______________;
②配平后的化学方程式是 ________________________________ 。
(4)O3 可由臭氧发生器(原理如图8所示)电解稀硫酸制得。
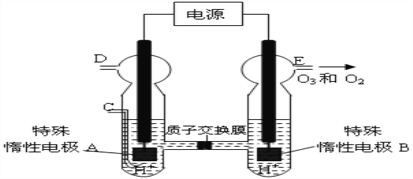
图中阴极为______(填“A”或“B”)。
若C处不通入O 2 ,D、E处分别收集到11.2L和4.48L气体(标准状况下), 则E处收集的气体中O3所占的体积分数为___________(忽略 O 3 的分解)。
③若C处通入O 2,则A极的电极反应式为:________________________________。
【答案】H2O2+2I-+2H+==I2+2H2O![]() -(5a-0.5b)kJ·mol-1KOHO3+2KI+H2O=2KOH+I2+O2A50%O2+4H++4e-=2H2O
-(5a-0.5b)kJ·mol-1KOHO3+2KI+H2O=2KOH+I2+O2A50%O2+4H++4e-=2H2O
【解析】(1). 根据化合价邻位转化规律可判断,在酸性条件下双氧水被还原为水,而碘离子被 氧化为碘单质,所以化学方程式为:H2O2+2I-+2H+==I2+2H2O
(2).三种过氧化物中只有过氧化钡可与硫酸反应生成难溶物硫酸钡,所以最适合的 就是过氧化钡了,其电子式为![]()
(3). 3.6 g碳的物质的量为0.3mol,6.4 g氧气的物质的量为0.2mol,它们之间恰好反应的热化学方程式为:3C(s)+2O2(g)=CO2(g)+2CO (g) △H1= -10a kJ/mol 。12.0gC完全燃烧的热化学方程式为:C(s)+O2(g) = CO2(g) △H2= -b kJ/mol 。根据盖斯定律可得:C(s)+![]() O2(g)===CO(g) ΔH=
O2(g)===CO(g) ΔH=![]() ( △H1 - △H2 ) = -(5a-0.5b)kJ/mol
( △H1 - △H2 ) = -(5a-0.5b)kJ/mol
所以 w=-(5a-0.5b)kJ/mol .臭氧中氧元素的化合价为0,它被还原后化合价降低为-2,所以还原产物为KOH,该反应的化学方程式配平后为:O3+2KI+H2O=2KOH+I2+O2
(4). 根据图中信息可知,电解稀硫酸时,惰性电极B上得到了氧气和臭氧,氧元素的化合价升高发生了还原反应,该电极一定是阳极,所以惰性电极A一定是阴极,若C处不通入O2,则D处收集到的气体为H2,11.2L在标准状况下为0.5mol,转移电子数为1mol,所以阳极上失去1mol电子后得到标准状况下的氧气、臭氧混合气4.48mol,物质的量为0.2mol,即n(O2)+n(O3)=0.2mol,再根据电子转移可得4n(O2)+6n(O3)=1mol,联立两式为方程组,可解得n(O3)=0.1mol,占总量一半,所以其体积分数为50% ;若C处通入O2,则A电极的电极反应式为:O2+4H++4e-=2H2O


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(8分)苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果醋是一种常见的有机酸,其结构简式为:
![]()
(1)苹果醋中含有的官能团的名称是 ;
(2)苹果醋的分子式为 ;
(3)1 mol苹果醋与足量金属钠反应,能生成标准状况下的氢气 L;
(4)苹果醋可能发生的反应是 。
A.与NaOH溶液反应 B.与石蕊溶液作用
C.与乙酸在一定条件下酯化 D.与乙醇在一定条件下反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+ , 下列物质中最好选用( )
A.H2O2溶液
B.KMnO4溶液
C.Cl2水
D.HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
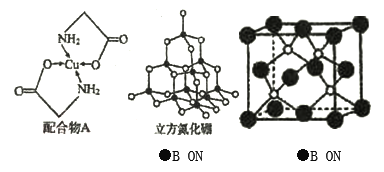
【题目】已知铜的配合物A(结构如图)。请回答下列问题:
(1)Cu的简化电子排布式为___________________。
(2)A中配位原子是_________,配位原子的第一电离能由大到小顺序为_________,杂化轨道类型均为_______________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中α键和π键数目之比是_________;N2O与CO2互为等电子体,且N2O分子中0只与一个N相连,则N2O的电子式为_________。
(4)在Cu催化下,甲醇可被氧化为甲醛(HCHO),甲醛分子中H—C—O的键角_________(选填“大于”、“小于”或“等于”)120。甲醇沸点_________甲醛(选填“大于”、“小于”或“等于”),原因是_________。
(5)立方氮化硼与金刚石结构相似,是超硬材料。立方氮化硼的晶胞如图所示,N填充在由B组成的四面体空隙中,则N原子半径RN最大为_________(用B原子半径RB和晶体边长a表示),立方氮化硼晶体内B—N键数与硼原子数之比为_________。结构化学上用原子坐标参数表示晶胞内部各原子的相对位置,下图(右)立方氮化硼的晶胞中,B原子的坐标参数分别有:B(0,0,0);B(l/2,0,l/2);B(l/2,l/2,0)等。则距离上述三个B原子最近且等距的N原子的坐标参数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色的酸性溶液中可以大量共存的离子组是( )
A.Fe2+ NO3﹣ I﹣ SO42﹣
B.MnO4﹣ K+ NO3﹣Na+
C.K+ Al3+ Cl﹣ SO42﹣
D.Mg2+ SO32﹣ Br﹣ Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:

(1)浸锰过程中Fe2O3与SO2反应的化学方程式为Fe2O3+ SO2+2H+=2Fe2++ SO42-+ H2O,该反应是经历以下两步反应实现的。写出ⅱ的离子方程式:_____________。
ⅰ:Fe2O3 + 6H+ = 2Fe3++3H2O
ⅱ:……
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为_____________(填离子符号)。
(3)写出氧化过程中MnO2与SO2反应的化学方程式:_________________。
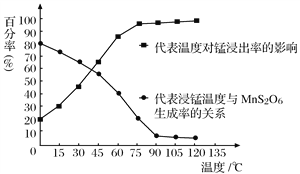
(4)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是_________;向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度不宜太高的原因是___________________。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:___________________。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关非金属及其化合物的说法正确的是( )
A.硅酸可使紫色石蕊试液变红色
B.二氧化硫通入紫色石蕊试液中.试液先变红后褪色
C.可用锌粒与稀硝酸反应制备氢气
D.液溴易挥发,所以存放液溴的试剂瓶中应加水封保存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com