
����һ����������Na2SO3��Ʒag��Ϊ�˲ⶨ����Na2SO3��������������������·�����������������������
A. ����Ʒ���Ƴ���ҺV1L��ȡ����25.00 mL�ñ�KMnO4��Һ�ζ������ı�KMnO4��ҺV2 mL
B. ����Ʒ�м�����H2O2���ټ�����BaCl2��Һ�����ˣ�������ϴ�ӡ��������������Ϊb g
C. ����Ʒ������ϡ�����ַ�Ӧ���ټ�������BaCl2��Һ�����ˣ�������ϴ�ӡ��������������Ϊc g
D. ����Ʒ������ϡ�����ַ�Ӧ�����ɵ���������ͨ��ʢ�б���NaHSO3��ϴ��ƿ��ʢ��ŨH2SO4��ϴ��ƿ��ʢ�м�ʯ�ҵĸ���ܢ�ʢ�м�ʯ�ҵĸ���ܢⶨ����ܢ�����d g
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ù�����H2SO4NaOH��NH3��H2O��NaCl����Һ������ͼ��ʾ����ֿ��������ӣ�����Һ�١��ڡ��ۡ�����(����)

A����NaCl����NaOH����NH3��H2O����H2SO4
B����H2SO4����NaOH����NH3��H2O����NaCl
C����H2SO4����NH3��H2O����NaOH����NaCl
D����NaCl����NH3��H2O����NaOH����H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ӱ������еõ�һ����A(C10H16)���Ц�����������A��ط�Ӧ���£�
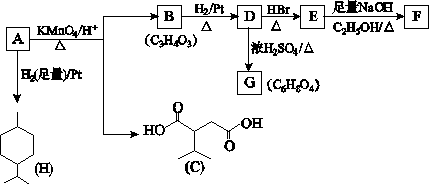
 | |||
 | |||
��֪�� 
(1)H�ķ���ʽΪ____________��
(2)B���������ŵ�����Ϊ____________��
(3)��������COOCH3���ŵ�C��ͬ���칹�干��________��(�����������칹)�����к˴Ź������׳���2�����շ���칹��Ľṹ��ʽΪ______________��
(4)B��D��D��E�ķ�Ӧ���ͷֱ�Ϊ______________��____________��
(5)GΪ����Ԫ���Ļ����д����ṹ��ʽ��______________��
(6)F��һ�������·����ۺϷ�Ӧ�ɵõ�һ�ָ���ˮ����֬������֬����Ϊ___________��
(7)д��E��F�Ļ�ѧ��Ӧ����ʽ��_________________________��
(8)A�Ľṹ��ʽΪ____________��A������ʵ�����Br2���мӳɷ�Ӧ�IJ��ﹲ��________��(�����������칹)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ⷨ�������Ժ�����ˮ����Ҫ����Cr2O72-��ʱ�����������������������������д��ڷ�ӦCr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O�����Cr3+��Cr��OH��3��ʽ��ȥ������˵������ȷ����
A. ������ӦΪFe-2e-=Fe2+
B. ����������ҺpH����仯
C. ��������Fe��OH��3��������
D. ��·��ÿת��12 mol���ӣ������1 mol Cr2O72-����ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڽ���������˵������ȷ����

A. ͼ1����������������������ͼ2����ӵ�������������
B. ���ֱ�������ͬ���DZ������ĸ�բ���Ͼ�Ϊ��������
C. ͼ1�еĸ�����Ӧ��Zn-2e-=Zn2+
D. ͼ2�и�բ�ű��淢����ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Na2SO3��һ����Ҫ����ԭ�ϡ�
��1����1.0 moL��L��Na2SO4��Һ�еμӷ�̪����Һ��Ϊ��ɫ�������ӷ���ʽ������ԭ��________________________��
��2����ҵ��Na2SO3���������������е�SO2��������ͨ��1L 1.0 mol��L��Na2SO3��Һ����ҺpH���ϼ�С������ҺpHԼΪ6ʱ������SO4�����������½���Ӧ�����ռ����д�����
�ٵ������ռ�������8.96 L SO2������ɱ�״��������ʱ��Һ��c��CO32-����c��HSO3-��=_________��
����ͼΪ��ͬ������Ͳ�ͬŨ�ȵ�Na2SO3������Ч�ʵ�Ӱ�졣

����˵���У���ȷ���� ��
a. Na2SO3Ũ��Խ������Ч��Խ��
b. ��ͬ�����£������������NaOH������Ч�����
c. ������ͬŨ�ȵ�Na2SO3��Һ���¶�Խ������Ч��Խ��
d. ����ҺpHԼΪ6ʱ����ʱ������Һ������ֻ��NaHSO2
����Һ���������½����м���������ͬʱ�õ�Ũ��SO2�����������Ļ�ѧ����ʽ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������ʣ�����ˮ���ڰ�ˮ����Ũ������������ƣ����壮���б��뱣������ɫƿ�����(����)
A��ȫ������
B���٢ۢݡ���
C���٢ۡ���
D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ѧ��ȤС���û��յ�þ���Ͻ���ȡ����������10.8 gþ���Ͻ�����˵����ȷ����(����)
A��������������18 mol/L H2SO4��Һ��Ӧ�����ɷų�0.6 mol H2
B��������������2 mol/L HNO3��Һ��Ӧ�����ٿɷų�0.45 mol H2
C��������������2 mol/L H2SO4��Һ��Ӧ���ų�H2�����ʵ�����0��0.45 mol֮��
D��������������2 mol/L NaOH��Һ��Ӧ���ų�H2�����ʵ�����0��0.6 mol֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݻ�ΪVL���ܱ������з���2LA��1LB��3A(g)+B(g)nC(g)+2D(g)���ﵽƽ���A���ʵ�������1/2����������ƽ��Ħ����������1/8����÷�Ӧ��n��ֵ�� ��
A�� 1 B�� 2 C�� 3 D�� 4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com