
|
已知:在 pH值为4左右的环境中,Ca2+、Fe2+几乎不水解,而Fe3+几乎完全水解.工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解.欲除去溶液中的杂质离子,下述方法中可行的是 | |
| [ ] | |
A. |
加入纯 Cu将Fe2+还原为Fe |
B. |
向溶液中通入 H2S使Fe2+沉淀 |
C. |
向溶液中通入 Cl2,再通入NH3,调节pH值为4左右 |
D. |
向溶液中通入 Cl2,再加入纯净的CuO粉末,调节pH值为4左右 |
科目:高中化学 来源: 题型:
 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:| O | - 3 |
| O | - 3 |
| O | 2- 3 |
| O | - 3 |
| O | 2- 3 |
| O | 2- 3 |
| O | - 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| [CO] | [CO2] |
查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高二化学 山东科学技术出版社 鲁教版 题型:058
在中性或碱性溶液中Na2SO3与S可以顺利反应合成大苏打(Na2S2O3·5H2O);反应的化学方程式如下:Na2SO3+S+5H2O=Na2S2O3·5H2O
现用Na2S和Na2CO3的混合液.Na2SO3固体.稀硫酸等试剂合成大苏打,按下列要求回答问题:
(1)制取SO2的化学方程式为________.
(2)反应过程中溶液的pH值逐渐下降,同时有S生成的化学方程式是:
①________________.
②________________.
③________________.
(3)合成大苏打时,Na2S与Na2CO3的最适宜的物质的量之比为________.
(4)当溶液的pH值下降到7左右,在加热条件下,溶液变为无色澄清时,欲得Na2S2O3·5H2O晶体,可采取的措施是________.
①趁热过滤 ②蒸发浓缩后冷却结晶
(5)在图所示的方框中画出发生气体的实验装置示意图(包括反应时容器中的物质),已知气流方向从左到右.
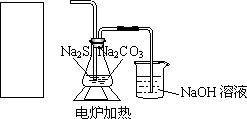

②铁架台、石棉网、酒精灯、玻璃导管之间的连接等,在示意图中不必画出.如需加热可在需要加热的仪器下方标出“Δ”.
查看答案和解析>>
科目:高中化学 来源:2010年四川绵阳高考预测(综合题)化学卷 题型:填空题
(16分)金属单质及其化合物与工农业生产、日常生活有密切的联系。请回答下列问题:
(2)一定温度下,氧化铁可以与一氧化碳发生如下反应:
①该温度时,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,5 min后,生成了单质铁11.2 g,则这段时间内CO的反应速率为 ;
②达平衡后,若温度升高,的值增大,则Q 0(填“>”、“=”、“<”)。
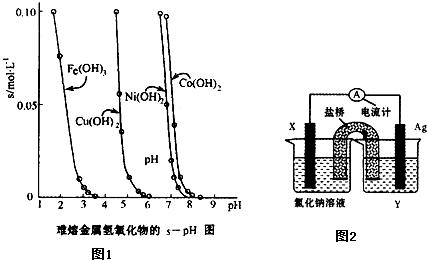
(3)工业常根据金属氢氧化物在酸中溶解度不同,通过控制溶液的pH,达到分离金属离子的目的。如是难溶金属的氢氧化物在不同pH下的溶解情况(s/mol·L-1)。若要除去CuCl2溶液的少量Fe3+,应控制溶液的pH为 (填序号)。 
A.小于l B.4左右 C.大于6 D.大于9
(4)某工业废水中含有Cu2+、Pb2+、Hg2+,若向工业废水中加入过量的FeS,当FeS、CuS、PbS和HgS共存时,溶液中c(Fe2+):c(Pb2+):c(Hg2+)= : : 。
已知:Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(PbS)=3.4×10-28mol2·L-2
Ksp(CuS)=1.3×10-36mol2·L-2,Ksp(HgS)=6.4×10-53mol2·L-2
(5)依据氧化还原反应:Cu2+(aq)+Fe(s)===Fe2+(aq)+Cu(s)设计成如图所示的原电池,则关于该电池装置的说法中不正确的是 (填序号)。
A.电极X的材料是Fe
B.电解质溶液Y是AgNO3溶液
C.原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中
D.原电池工作时,x电极反应为:O2+2H2O+4e-→4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
金属单质及其化合物与工农业生产、日常生活有密切的联系。请回答下列问题:

(2)一定温度下,氧化铁可以与一氧化碳发生如下反应:

①该温度时,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,5 min后,生成了单质铁11.2 g,则这段时间内CO的反应速率为 ;
②达平衡后,若温度升高,的值增大,则Q 0(填“>”、“=”、“<”)。
(3)工业常根据金属氢氧化物在酸中溶解度不同,通过控制溶液的pH,达到分离金属离子的目的。如是难溶金属的氢氧化物在不同pH下的溶解情况(s/mol·L-1)。若要除去CuCl2溶液的少量Fe3+,应控制溶液的pH为 (填序号)。

A.小于l B.4左右 C.大于6 D.大于9
(4)某工业废水中含有Cu2+、Pb2+、Hg2+,若向工业废水中加入过量的FeS,当FeS、CuS、PbS和HgS共存时,溶液中c(Fe2+):c(Pb2+):c(Hg2+)= : : 。
已知:Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(PbS)=3.4×10-28mol2·L-2
Ksp(CuS)=1.3×10-36mol2·L-2,Ksp(HgS)=6.4×10-53mol2·L-2
(5)依据氧化还原反应:Cu2+(aq)+Fe(s)===Fe2+(aq)+Cu(s)设计成如图所示的原电池,则关于该电池装置的说法中不正确的是 (填序号)。

A.电极X的材料是Fe
B.电解质溶液Y是AgNO3溶液
C.原电池工作时,盐桥中的阴离子不断移向左池的氯化钠溶液中
D.原电池工作时,x电极反应为:O2+2H2O+4e-→4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com