
| A. | 3mol | B. | 2.5mol | C. | 1mol | D. | 0.5mol |
科目:高中化学 来源: 题型:选择题
| A. | 将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变红,并能闻到刺激性气味 | |
| B. | 乙醇(CH3CH2OH)与二甲醚(CH3-O-CH3)互为同分异构体 | |
| C. | 在蛋白质溶液中加入饱和硫酸铵溶液,会使蛋白质发生变性 | |
| D. | 煤的干馏是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解时,石墨作阴极,不锈钢作阳极 | |
| B. | 电解时,阳极反应是:I--6e-+3H2O═IO3-+6H+ | |
| C. | 溶液调节至强酸性,对生产不利 | |
| D. | 电解后阴极周围溶液的pH升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  装置可用于比较NaHCO3和Na2CO3的稳定性 | |
| B. |  用酒精萃取溴水中的溴可选择装置 | |
| C. | 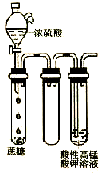 如图装置进行实验可看到酸性KMnO4溶液褪色 | |
| D. | 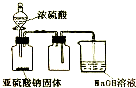 如图装置可用于实验室制取并收集少量SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
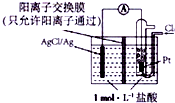
| A. | 正极为Pt电极,电极反应为2Ag++Cl2+2e-═2AgCl↓ | |
| B. | 放电时,交换膜两侧溶液中盐酸浓度不变 | |
| C. | 若用NaCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.01mole-时,交换膜左侧溶液中约减少0.02mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.44 kJ | B. | 44 kJ | C. | 88 kJ | D. | 330 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
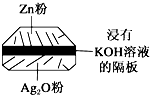 (1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{充电}^{放电}$2PbSO4+2H2O.请回答下列问题(不考虑氢、氧的氧化还原):
(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{充电}^{放电}$2PbSO4+2H2O.请回答下列问题(不考虑氢、氧的氧化还原):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验 | 操作 |
| A | 测定次氯酸钠的pH | 用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,变色后,与标准比色卡对比 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴快速流出 |
| D | 取出分液漏斗中所需的上层液体 | 将下层液体从分液漏斗下端管口放出后,关闭活塞,换一个接收容器,从分液漏斗下端管口继续放出下层液体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
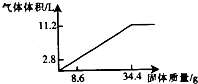 在100mlNaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热使之充分反应,下图表示加入固体的质量与产生气体的体积(标准状况)的关系,试回答:
在100mlNaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热使之充分反应,下图表示加入固体的质量与产生气体的体积(标准状况)的关系,试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com