
 在密闭容器中加入等浓度的CO与H2O,T℃时发生如下反应:
在密闭容器中加入等浓度的CO与H2O,T℃时发生如下反应:| △c |
| △t |
| 0.2-0.08 |
| 4 |
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| 0.12×0.12 |
| 0.08×0.08 |
| 9 |
| 4 |
| 9 |
| 4 |
| 总质量 |
| 总物质的量 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验1中CO2的体积为标准状况下,其它气体在同温同压下测定).
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验1中CO2的体积为标准状况下,其它气体在同温同压下测定). | 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
| 1 | 10mL 0.1mol/LNaOH溶液 | 22.4mLCO2 | 无明显现象 |
| 2 | 20mL H2S | 10mL SO2 | |
| 3 | 30mL NO2 | 10mL H2O(l) | 剩有无色气体,活塞自动向内压缩 |
| 4 | 15mL Cl2 | 40mL NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| B、c(Na+)═c(HCO3-)+c(CO32-) |
| C、c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-) |
| D、c(OH-)═c(H +)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
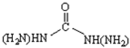 一种新型锅炉水添加剂的分子结构如图所示,该添加剂能除去锅炉水中溶解的氧气.下列有关说法正确的是( )
一种新型锅炉水添加剂的分子结构如图所示,该添加剂能除去锅炉水中溶解的氧气.下列有关说法正确的是( )| A、该添加剂与尿素[CO(NH2)2]互为同系物 |
| B、分子中各原子的最外层均达到八电子稳定结构 |
| C、分子中所有原子共平面 |
| D、该添加剂具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、充电电池的化学反应原理是氧化还原反应 |
| B、充电电池可以无限制地反复放电、充电 |
| C、充电是使放电时的氧化还原反应逆向进行 |
| D、较长时间不使用电器时,最好从电器中取出电池,并妥善存放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石墨电极上产生氢气 |
| B、铜电极发生还原反应 |
| C、铜电极接直流电源的负极 |
| D、当有0.1mol电子转移时,有0.1molCu2O生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com