
在电冶铝的电解槽中存在电解质W2[X2Y2Z4],己知四种元素的简单离子的电子层结构均相同,Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半,下列说法正确的是
A.原子序数:W>X>Y>Z
B.原子半径:r(w)>r(X)>r(Y)>r(Z)
C.W的最高价氧化物的水化物碱性比X的弱
D.Y的简单氢化物的稳定性比Z的强
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
硅被誉为无机非金属材料的主角。据2001年12月的《参考消息》报道,有科学家提出硅是“21世纪的能”、“未的石油”。下列有关说法正确的是
A.硅在地壳中含量居第二位,在地球上有丰富的硅资,如石英、水晶、玛瑙的主要成分都是单质硅
B.在野外,用硅、烧碱的混合物可以制取氢气
C.硅的性质稳定,不与任何酸反应
D.硅是一种良好的半导体材料,所以是制造光导纤维的基本原料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:填空题
(12分)钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧可获得钛酸钡粉体。
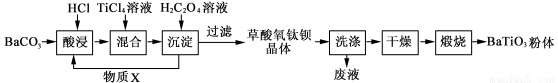
(1)酸浸时发生的反应的离子方程式为 ;为提高BaCO3的酸浸率,可采取的措施为 (任答一点)。
(2)配制TiCl4溶液时,通常将TiCl4溶于浓盐酸,目的是 。
(3)加入H2C2O4溶液时,发生反应的化学方程式为 ;
可循环使用的物质X是 。
(4)煅烧得到BaTiO3的同时,生成高温下的气体产物有CO、 和 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:填空题
[物质结构与性质]乙烯酮 (CH2=C=O)是一种重要的有机中间体,可由C2H2和O2的混合气体通过锌、钙、银的三种金属的氧化物(催化剂)反应得到。也可用CH3COOH在痕量(C2H5O)3P=O存在下加热脱H2O得到。
(1)Zn2+基态核外电子排布式为 。
(2)与H2O互为等电子体的一种阴离子为 ;乙烯酮分子中碳原子杂化轨道类型有 。
(3)CH3COOH的沸点比HCOOCH3的高,其主要原因是 。
(4)lmol(C2H5O)3P=O分子中含有的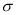 键的数目为 。
键的数目为 。
(5)Ag的氧化物的晶胞结构如图所示,
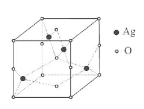
该氧化物的化学式为 .
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
一定温度下,在三个体积均为1.0L的恒容密闭容器中,充入一定量的H2和SO2发生下列反应:
3H2(g)+SO2(g)  2H2O(g)+H2S(g)
2H2O(g)+H2S(g)
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
H2 | SO2 | H2 | SO2 | ||
容器I | 300 | 0.3 | 0.1 | / | 0.02 |
容器II | 300 | 0.6 | 0.2 | / | / |
容器III | 240 | 0.3 | 0.1 | / | 0.01 |
下列说法正确的是
A.该反应正反应为吸热反应
B.容器II达到平衡时SO2的转化率比容器I小
C.容器III达到平衡的时间比容器I短
D.240℃时,该反应的平衡常数为1.08×104L? mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
下列物质性质与应用对应关系正确的是
A.钠和钾的合金具有导电性,可用于快中子反应堆热交换剂
B.明矾溶于水能产生Al(OH)3胶体,可用作净水剂
C.甲醛能使蛋白质变性,可用于食品防腐剂
D.水玻璃易溶于水,可用于生产黏合剂和防火剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:实验题
(15分)碘化钠是实验室中常见的分析试剂,常用于医疗和照相业。工业上通常用水合肼(N2H4·H2O,100℃以上分解)还原法制取碘化钠,工艺流程如下:
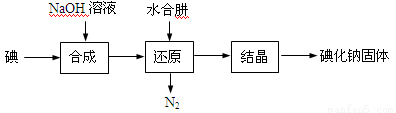
(1)合成过程的反应产物中含有IO3-,写出合成过程的离子方程式 。
(2)还原过程必须保持反应温度在60~70℃,这个温度既能保证反应的快速进行,又能 。工业上也可以用Na2S或Fe屑还原制备碘化钠,但水合肼还原法制得的产品纯度更高,原因是 。
(3)请补充完整检验还原液中是否含有IO3-的实验方案:取适量还原液, 。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液。
(4)测定产品中NaI含量的实验步骤如下:
a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中;
c.用0.1000mol·L-1AgNO3溶液滴定至终点,记录消耗AgNO3溶液的体积;
d.重复b、c操作2~3次,记录相关实验数据。
①滴定过程中,AgNO3溶液应放在 中;步骤d的目的是 。
②若用上述方法测定产品中的NaI含量偏低(忽略测定过程中的误差),其可能的原因是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:选择题
下列有关化学用语的表示正确的是
A.NH4Cl的电子式: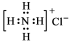 B.Cl-的结构示意图:
B.Cl-的结构示意图:
C.中子数为21的钾原子:40 19K D.对硝基苯酚的结构简式: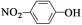
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省深圳市高三第一次调研考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.将高温水蒸气通过炽热的铁粉,铁粉变红色
B.向Fe(OH)3胶体中滴加稀H2SO4,先出现沉淀,后沉淀溶解
C.将市售食盐溶于水,滴加淀粉溶液不变蓝色,说明不是加碘盐
D.Cu的金属活泼性比Fe弱,故水库铁闸门上接装铜块可减缓铁腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com