
����A��B��C��D��E��F��G��ƿ��ͬ���ʵ���Һ�����Ǹ���Na2CO3��Na2SO4��KCl��AgNO3��MgCl2��Cu(NO3)2��Ba(OH)2��Һ��һ�֡�Ϊ�˼��𣬸�ȡ������Һ����������ϣ�ʵ�������±���ʾ�����С�������ʾ���ɳ����������������ʾ�۲첻�����Ա仯��
A | B | C | D | E | F | G[m] | |
A | �� | �� | �� | �� | �� | �� | �� |
B[ | �� | �� | �� | ��] | �� | �� | �� |
C | �� | �� | �� | �� | �� | �� | �� |
D | �� | �� | �� | �� | �� | �� | �� |
E | �� | �� | �� | �� | �� | �� | �� |
F | �� | �� | �� | �� | �� | �� | �� |
G | �� | �� | �� | �� | �� | �� | �� |
��д���й����ʵĻ�ѧʽ��A�� ��C�� ��E�� ��G�� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��ݸ����У������ѧ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�õ������ҺΪ��������ˮ��Һ������ȼ�ϵ�ص�ⱥ����������Һһ��ʱ�䣬������ʱ�¶Ȳ������ö��Ե缫������˵������ȷ����
A������ظ������� ����ʱ������������
����ʱ������������ ��������
��������
B�����ص�������ӦʽΪ��4OH--4e-=2H2O+O2��
C������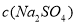 ���䣬����Һ���о�������
���䣬����Һ���о�������
D�������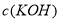 ���䣻��������Һ
���䣻��������Һ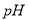 ���
���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
0.8 gij�����к���3.01��1022�����ӣ������ʵ���Է���������
A��16 B��16 g C��32 D��32 g/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���в���ȷ����
�� ����ͭ�������õĵ����ԣ����Ե繤���� ʱ������ͭ�ߺ����߽ʽ���һ��
ʱ������ͭ�ߺ����߽ʽ���һ��
�� ����β���к�������Ⱦ�����ĵ��������ԭ��������ȼ�ղ����
�� �����Ʊ���Cu��OH��2����Һ�벡����Һ���ȣ��ɼ��鲡����Һ���Ƿ��������ǣ�
�� ij��ˮ��Ʒ�ɼ������һ��ʱ�䣬pHֵ��4.68��Ϊ4.28������Ϊˮ���ܽ��˽϶��CO2
�� �����������ھ�ˮ�� ��Ҫ�����������ӿ���ˮ��õ�����������
��Ҫ�����������ӿ���ˮ��õ�����������
�ޡ�ˮ��ʯ������Ҫ���ܽ���CO2����ˮ��CaCO3�������������˿����Ե�Ca��HCO3��2��Ե�ʡ�
A���ڢۢ� B���٢ڢ� C.�ۢܢ� D���ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������人����ʦ��һ���еȰ�У����������һ����ѧ�������� ���ͣ�ʵ����
������������Ļ�ѧʽΪFeC2O4��2H2O������һ�ֵ���ɫ�ᾧ��ĩ�������̼��ԣ�����ʱ�ɷ������·ֽⷴӦ��FeC2O4��2H2O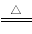 FeO +CO2��+CO��+H2O
FeO +CO2��+CO��+H2O
��1����������ͼ���ṩ�������������ظ�ѡ�ã���ÿ����������ѡ��һ�Σ���ѡ���Ҫ���Լ�[��ѡ����Լ���NaOH��Һ������ʯ��ˮ������̼������Һ��CuO����ˮ����ͭ�����Ը��������Һ]�����һ��ʵ�飬����FeC2O4��2H2O����ʱ�ֽ��������̬�������ˮ�����������ּ���װ�úͼг�������ͼ����ȥ�����ڴ������д�±������Բ���������Ҳ���Բ��䣩��
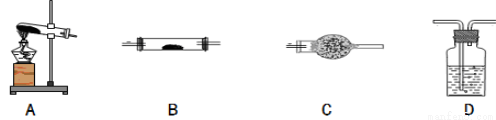
�������� | �������������� | ���� |
A | ������������ | ���Ȳ�����������õ�������� |
D | NaOH��Һ | |
��2��������Ŀ�ṩ��װ�ú�Ҫ����Ƶ�ʵ�����Դ��ڵ�һ�������� ��
��3����Ӧ��������Aװ���Թ����к�ɫ�����ĩ����������������ʱ����ȼ����������������Ŀ���ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭��Ҧ��ѧ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����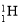 ��
��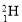 ��
��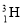 ��H+��H2����֮����
��H+��H2����֮����
A���������ͬλ�� B��������Ԫ��
C��������ֺ��� D����Ԫ�ص����ֲ�ͬ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭̨����ѧ�߶��ϵ�����ͳ����ѧ�Ծ��������棩 ���ͣ�ѡ����
��25��ʱ��������Һ��pHֵ��С����
A��0.01mol��L-1HCl
B��pH=2��H2SO4��Һ
C��c(OH)=10-13 mol��L-1
D��pH=1��Һ��ˮϡ��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����ϳ����и߶�12���¿���ѧ���������棩 ���ͣ�ѡ����
���й����Ȼ�ѧ��Ӧ����ʽ��������ȷ����
A��HCl��NaOH��Ӧ���к��ȡ�H=-57��3kJ��mol-1����H2SO4��Ca(OH)2��Ӧ���к��ȡ�H=2����-57��3��kJ��mol-1
B��CO(g)��ȼ������283��0 kJ��mol-1����2 CO2 (g)= 2CO(g)+O2(g)�ķ�Ӧ�ġ�H=+(2��283��0) kJ��mol-1
C����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
D����mol����ȼ��������̬ˮ��CO2���ų��������Ǽ����ȼ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ׯ���и߶�10��ѧ����黯ѧ���������棩 ���ͣ������
�о���ѧ��Ӧ�е������仯����Ҫ���塣�����ѧ��֪ʶ�ش��������⣺
��1����֪һ����̼��ˮ������Ӧ���̵������仯����ͼ��ʾ��

�ٷ�Ӧ���Ȼ�ѧ����ʽΪ____________________________________________��
����֪��
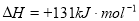
��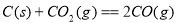
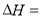
��2����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ������γɣ����1 mol��ѧ��ʱ�ͷţ������գ�����������֪��N��N���ļ�����948.9kJ��mol��1��H��H���ļ�����436.0 kJ��mol��1�� N��H���ļ�����391.55 kJ��mol��1����1/2N2(g) + 3/2H2(g) == NH3(g) ��H = ��
��3����ͼ��һ����ѧ���̵�ʾ��ͼ������֪�������Һ��������

�ټ�װ����ͨ��CH4�ĵ缫��ӦʽΪ
��һ��ʱ�䣬�������в���11.2L����״���£�����ʱ�����ҳ��в�����������ʵ���Ϊ ����Ҫʹ���ػָ����ǰ��״̬��Ӧ������м��� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com