
| A. | 化学反应速率是指一定时间内任何一种反应物浓度的减小或任何一种生成物浓度的增加 | |
| B. | 化学反应速率为“0.8 mol•L-1•s-1”所表示的意思是:时间为1 s时,某物质的浓度为0.8 mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的快慢 | |
| D. | 对于任何化学反应来说,反应现象越明显,反应速率越大 |
分析 A.化学反应速率为单位时间内浓度的变化量;
B.化学反应速率为平均速率;
C.化学反应速率即为描述化学反应快慢的物理量;
D.反应速率与现象无关.
解答 解:A.化学反应速率为单位时间内浓度的变化量,则化学反应速率通常用单位时间内反应物浓度的减小或生成物浓度的增大来表示,固体或纯液体的浓度变化视为0,故A错误;
B.因化学反应速率为平均速率,则化学反应速率为0.8mol/(L•s)是指1s内该物质的浓度变化量为0.8mol/L,故B错误;
C.化学反应速率是描述化学反应快慢的物理量,根据化学反应速率可以知道化学反应进行的快慢,故C正确;
D.反应速率与现象无关,反应速率快的,现象可能明显,也可能不明显,故D错误,
故选C.
点评 本题考查化学反应速率,为高频考点,侧重于学生的分析能力的考查,明确化学反应速率的定义及计算表达式、化学反应速率的理解等即可解答,选项B为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KCl=K++Cl- | B. | H2CO3?2 H++CO32- | ||
| C. | H2SO4=2H++SO42- | D. | Ba(OH)2=Ba2++2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
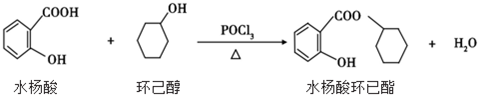
| A. | 水杨酸的核磁共振氢谱有 4 个吸收峰 | |
| B. | 水杨酸、环已醇和水杨酸环已酯都能与 FeCl3 溶液发生显色反应 | |
| C. | 1mol 水杨酸跟浓溴水反应时,最多消耗 2molBr2 | |
| D. | 1mol 水杨酸环已酯在 NaOH 溶液中水解时,最多消耗 3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取Fe(OH)3胶体:Fe3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 锅炉除水垢时先用纯碱浸泡:CaSO4+CO32-═CaCO3+SO42- | |
| C. | 泡沫灭火器灭火原理:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| D. | 向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O═CO32-+2C6H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4和Ba(OH)2 | B. | CO2和NaOH | C. | CaCO3和HCl | D. | Mg(OH)2和CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
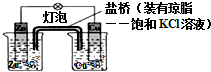
| A. | 正极表面出现气泡 | B. | 电池反应:Zn+Cu2+=Zn2++Cu | ||
| C. | 在外电路中,电流从负极流向正极 | D. | 盐桥中K+移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的电流方向是由锌到二氧化猛 | |
| B. | 该电池反应中MnO2起催化作用 | |
| C. | 当0.1molZn完全溶解时,流经电解液的电子个数为1.204×1023 | |
| D. | 电池正极反应为MnO2+e-+H2O═MnO(OH)+OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com