
| A、氨气易液化,液氨气化时吸热,因此液氨常用作制冷剂 |
| B、氮的固定是指将游离态的氮转变为氮的化合物 |
| C、漂白粉和漂粉精的有效成分都是Ca(CIO)2 |
| D、SO2和CO2都是造成酸雨的主要气体 |


科目:高中化学 来源: 题型:
| A、弱电解质的电离平衡常数受温度影响,与溶液浓度无关 |
| B、电离平衡常数表达了弱电解质的电离能力 |
| C、多元弱酸水溶液中的H+主要是第一步电离产生的 |
| D、由于Ka[HF]>Ka[CH3COOH]>Ka[HCN],所以酸性顺序HF<CH3COOH<HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | F-D | F-F | B-B | F-B | C═D | D═D |
| 键能/kJ?mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(B2)=0.6mol/(L?s) |
| B、v(A2)=0.5mol/(L?s) |
| C、v(C)=0.45mol/(L?s) |
| D、v(B2)=2.4mol/(L?min). |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2+2H2O+4e-=4OH- |
| B、2H++2e=H2↑ |
| C、4 OH-=2H2O+O2+4e- |
| D、Fe=Fe2++2e- |
查看答案和解析>>
科目:高中化学 来源: 题型:
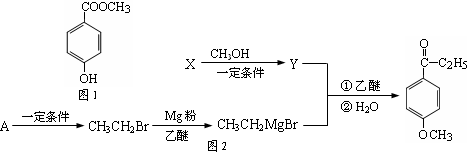
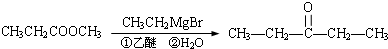
 )是食品添加剂的增香原料,其合成路线如图:
)是食品添加剂的增香原料,其合成路线如图: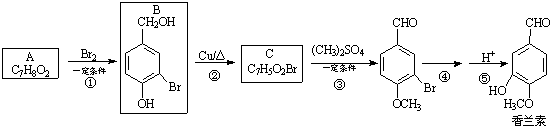

| (CH3)2SO4 |
| 一定条件 |
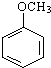
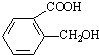 ,在一定条件下可以合成聚酯高分子,写出该聚酯高分子的结构简式
,在一定条件下可以合成聚酯高分子,写出该聚酯高分子的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com