
下列化学用语书写正确的是( )
A.熔融状态下NaHSO4电离方程式:NaHSO4=Na++H++SO42-
B.碳酸氢铵溶液中加入足量氢氧化钠:HCO + OH-=CO32-+ H2O
+ OH-=CO32-+ H2O
C. 钠投入水中:2Na+2H2O=2Na++2OH-+H2↑
D.氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
科目:高中化学 来源: 题型:
氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解。请你和他一起通过下图所示Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
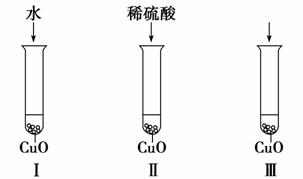
(1)某同学提出的假设是_________________________________。
(2)通过实验Ⅰ可以证明_________________________________。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步确认的实验操作是:在Ⅲ中先加入________,再加入________。
(4)探究结果为__________________________________________。
(5)反应的离子方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
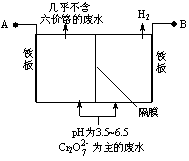
电解法处理含铬(六价铬)废水的原理如图所示,阳极区溶液中的离子反应是Cr2O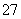 +6Fe2++14H+ == 2Cr3+ +6Fe3+ 7H2O。下列说法正确的是
+6Fe2++14H+ == 2Cr3+ +6Fe3+ 7H2O。下列说法正确的是
A.电解槽中H+向阳极移动
B.阳极的电极反应式是:Fe-3e-= Fe3+
C.电解一段时间后,阴极区溶液的pH升高
D.阳极的铁板可用石墨代替
查看答案和解析>>
科目:高中化学 来源: 题型:
对于某些物质或离子的检验及结论一定正确的是( )
A.某物质的水溶液使红色石蕊试纸变蓝,该物质一定是碱
B.某气体能使湿润淀粉碘化钾试纸变蓝,该气体一定是氯气
C.某物质的水溶液中加入盐酸产生无色无味气体,该溶液一定含有碳酸根离子
D.往铁和稀硝酸反应后的溶液中滴入KSCN溶液,溶液显血红色,则该反应后的溶液中肯定有Fe3+,可能还有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )

| A.图(a)中,随着电解的进行,溶液中H+的浓度越来越小 |
| B.图(b)中,Mg电极作电池的负极 |
| C.图(c)中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D.图(d)中,K分别与M、N连接时,Fe电极均受到保护 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:
2CO2(g)+6H2(g)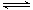 CH3OCH3(g)+3H2O(g) △H>0。
CH3OCH3(g)+3H2O(g) △H>0。
①写出该反应的平衡常数表达式 。
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是 。
A.容器中密度不变
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚
C.v(CO2)︰v(H2)=1︰3
D.容器内压强保持不变
(2)汽车尾气净化的主要原理为:2NO(g)+2CO (g) 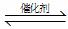 2CO2 (g) +N2 (g) 。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) +N2 (g) 。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
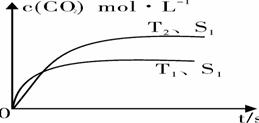
① 该反应的ΔH 0(选填“>”、“<”)。
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(3)已知:CO(g)+ 2H2(g)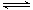 CH3OH(g)△H = -a kJ•mol-1。
CH3OH(g)△H = -a kJ•mol-1。
①经测定不同温度下该反应的平衡常数如下:
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4 mol·L-1、c(H2)=0.4 mol·L-1、c(CH3OH)=0.8 mol·L-1, 则此时v正 v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
达到平衡时CO的转化率为 。
(4)氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产。用0.10mol·L—1盐酸分别滴定20.00mL0.10mol·L—1的NaOH溶液和20.00mL0.10mol·L—1氨水所得的滴定曲线如下:
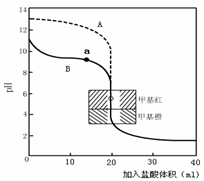
请指出盐酸滴定氨水的曲线为 (填A、B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序 。
(5)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧实验验中相关的反应有:
4NH3(g)+3O2(g)= 2N2(g)+6H2O(l) △H1 ①
4NH3(g)+5O2(g)= 4NO(g)+6H2O(l) △H2 ②
4NH3(g)+6NO(g)= 5N2(g)+6H2O(l) △H3 ③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= 。
(6)美国Simons等科学家发明了使NH3直接用于燃料电池的方法,其装置为用铂作为电极,加入电解质溶液中,其电池反应为 4NH3+3O2=2N2+6H2O。写出该燃料电池的负极反应式 。
(7)已知 :难溶电解质Cu(OH)2在常温下的Ksp=2×10-20,则常温下:
①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。
②要使0.2 mol·L-1 CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在天平的左右两个托盘上放有两个烧杯,两个烧杯中分别盛有盐酸和氢氧化钠溶液,天平处于平衡状态,当分别向两烧杯中加入等质量的铝(酸和碱都是足量的)充分反应后( )
A.天平保持平衡 B.左高右低 C.左低右高 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象或应用中,不能用胶体知识解释的是 ( )
A.在饱和FeCl3溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.实验时手指不慎划破,可从急救箱中取出FeCl3溶液止血
C.清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱
D.向豆浆中加入硫酸钙可制成可口的豆腐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com