
分析 (1)电解质是指:在水溶液中或熔融状态下能够导电的化合物;
(2)非电解质是指:在熔融状态和水溶液中都不能导电的化合物,非电解质在熔融状态和水溶液中自身都不能离解出自由移动的离子;
(3)强电解质一般是强酸、强碱和活泼金属氧化物以及大部分盐,它们溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物;
(4)一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价键化合物.
解答 解::①烧碱固体为氢氧化钠,溶于水或者熔融状态时,可以完全电离成氢氧根离子和钠离子,属于强电解质,氢氧根离子和钠离子之间存在离子键,所以属于离子化合物;
②铁丝是铁单质,它既不是电解质也不是非电解质;
③氯化氢气体溶于水,完全电离成氯离子和氢离子,属于强电解质,氯原子和氢原子之间存在共价键,属于共价化合物;
④稀硫酸为硫酸的水溶液,为混合物,它既不是电解质也不是非电解质;
⑤SO2在水溶液中与水反应生成亚硫酸,亚硫酸电离出自由移动的氢离子和亚硫酸根离子导电,SO2自身不能电离,SO2是非电解质,硫原子和氧原子之间存在共价键,属于共价化合物;
⑥H2CO3 为二元弱酸,分步电离,H2CO3?HCO3-+H+,第二步为:HCO3-?CO32-+H+,属于弱电解质,各种原子之间只存在共价键,属于共价化合物;
⑦熔融氯化钠,可以完全电离变成氯离子和钠离子,属于强电解质,氯离子和钠离子之间存在离子键,所以属于离子化合物;
故答案为:(1)①③⑥⑦(2)⑤(3)①③⑦(4)①⑦、③⑤⑥.
点评 本题考查了电解质和非电解质的判断及离子化合物和共价化合物的判断,注意能导电的物质不一定是电解质,共价化合物中一定不含离子键,离子化合物中可能含有共价键,为易错点,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 | |
| B. | S(g)+O2(g)═SO2 (g)△H1 S(s)+O2(g)═SO2 (g)△H2 | |
| C. | C(s)+O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | HCl(g)═H2(g)+Cl2(g)△H1 2HCl(g)═H2(g)+Cl2(g)△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | SO2通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | SO2具有还原性 |
| B | 向NaSiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| C | 将盛有铜片的容器中加入浓硝酸 | 产生大量红棕色气体;溶液变为蓝绿色 | 浓硝酸具有强氧化性 |
| D | 浓硫酸滴到湿润的蔗糖中 | 蔗糖变成黑色海绵状 | 浓硫酸具有脱水性和强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

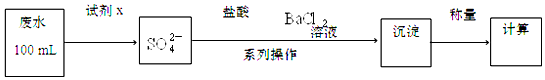
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 取少量待检验溶液,向其中加入少量新制氯水,在滴加KSCN溶液,溶液呈血红色 | 待测液中含有Fe3+ |
| B | 室温下,向浓度均为0.1mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. | Ksp(Ba2SO4)<Ksp(Ca2SO4) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
| D | 室温下,用PH试纸测得:0.1mol•L-1 Na2SO3溶液的PH约为10;0.1mol•L-1 NaHSO3溶液的PH约为5 | HSO3-结合H+的能力比SO32-的强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{94}^{239}$Pu与${\;}_{94}^{238}$Pu互为同位素 | |
| B. | ${\;}_{94}^{239}$Pu原子核外有94个电子 | |
| C. | ${\;}_{94}^{239}$Pu原子核中有94个中子 | |
| D. | ${\;}_{94}^{239}$Pu与${\;}_{92}^{238}$U为两种不同核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
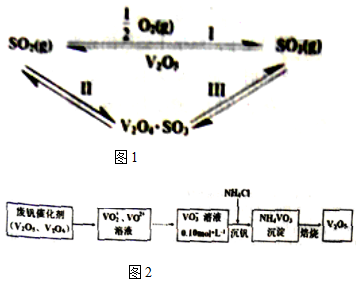
| 化学键 | S=O(SO2) | S=O(SO3) | O=O(O2) |
| 能量/kJ | 535 | 472 | 496 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,23gNO2和N2O4混合气体中含O原子数为NA | |
| B. | 1mol/L Al2(SO4)3溶液中含SO42-个数为3NA,含Al3+个数小于2NA | |
| C. | 在标准状况下,将22.4L SO3溶于水配成1L溶液,所得溶液中含SO42-个数为NA | |
| D. | 将1moL 氯气通入到足量水中,则N(HClO)+N(Cl-)+N(ClO-)═2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com