
| A�������������������ͭ���������Һ�ֱ����������Ȼ�����Һ��Ӧ�����������ᱵ������������ȣ���������������Һ�����ʵ���Ũ��֮��Ϊ1:1:1 |
| B��Na2O2��Na2O��0.1mol�ֱ����100gˮ�У�������Һ�����ʵ���Ũ�Ȳ���� |
| C�����������ֱ�Ϊ5%��15%�İ�ˮ�������Ϻ�������Һ����������Ϊ10% |
D��20��ʱ������KCl��Һ���ܶ�Ϊ1.174g?cm��3�����ʵ���Ũ��Ϊ4.0 mol?L��1�������Һ��KCl����������Ϊ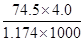 ��100% ��100% |
 mol��CuSO41 mol��K2SO41 mol����Ũ��֮��Ϊ
mol��CuSO41 mol��K2SO41 mol����Ũ��֮��Ϊ : 1 : 1="1" : 3 : 3��A�����B�Na2O2��Na2O��0.1mol�ֱ����100gˮ�У�������Һ���������ͬ�������ʵ���Ũ�Ȳ���ȣ�B�����C����,�����ְ�ˮ�������ϣ�Ũ���ܶȽ�С������������С�����ְ�ˮ��Ϻ������������ӽ�ϡ��ˮ��Ũ�ȣ����ð�ˮ��Һ����������С��10%��C�����20��ʱ������KCl��Һ���ܶ�Ϊ1.174g?cm-3�����ʵ���Ũ��Ϊ4.0mol?L-1������c=
: 1 : 1="1" : 3 : 3��A�����B�Na2O2��Na2O��0.1mol�ֱ����100gˮ�У�������Һ���������ͬ�������ʵ���Ũ�Ȳ���ȣ�B�����C����,�����ְ�ˮ�������ϣ�Ũ���ܶȽ�С������������С�����ְ�ˮ��Ϻ������������ӽ�ϡ��ˮ��Ũ�ȣ����ð�ˮ��Һ����������С��10%��C�����20��ʱ������KCl��Һ���ܶ�Ϊ1.174g?cm-3�����ʵ���Ũ��Ϊ4.0mol?L-1������c=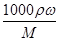 ��֪����������Ϊw=
��֪����������Ϊw=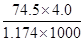 ��100%����D��ȷ��
��100%����D��ȷ��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�0��1molCl2����ˮ��ת�Ƶĵ�����ĿΪ0��1NA |
| B�����³�ѹ�£�16gO2��O3�Ļ�������к��е�ԭ������ΪNA |
| C����״���£�11.2LH2O�к��з��ӵ���ĿΪ0.5NA |
| D��2.4g����þ���þ����ʱʧȥ�ĵ�����ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1��b-2a��mol/L | B��10��2a-b��mol/L | C��10��b-a��mol/L | D��10��b-2a��mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1 mol Cl2������Fe��Ӧת�Ƶ�����һ��Ϊ3NA |
| B����״���£�2.24 L NH3�к��й��ۼ�����ĿΪNA |
| C��1 mol Na2O��Na2O2�����������������������3 NA |
| D������£�11.2L SO3�����ķ�����ĿΪ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.5mol?L��1 Fe2(SO4)3��Һ�к���SO42����Ϊ1.5NA |
| B��7.8g Na2O2����ˮ��������Һ�к���O22����ΪNA |
| C����״���£�22.4LCl2�����������۷�Ӧ��ת�Ƶĵ�����Ϊ3NA |
| D�����³�ѹ�£�7.0g��ϩ�ͱ�ϩ�Ļ�����к�����ԭ�ӵ���ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��21.2g | B��21.6g | C��22.0g | D��22.4g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2:1:2 | B��5:5:4 | C��1:1:1 | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��4.4 g��ȩ�����к��еĹ��õ��Ӷ���Ϊ0.6NA |
| B����״���£�11.2 L���ȼ�������������Ϊ0.5 NA |
| C��18.8 g�����к���̼̼˫���ĸ���Ϊ0.6 NA |
| D��������ϩ����ϩ����ϩ�Ļ�����干14g����ԭ����Ϊ3NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com