
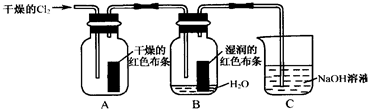
分析 (1)氯气能使湿润的有色布条褪色,但是不能使干燥的有色布条褪色,次氯酸具有漂白性,氯气没有漂白性;
(2)根据氯气和水反应的产物是盐酸和次氯酸,证明二者谁有漂白性即可;
(3)氯气有毒,可以用氢氧化钠来吸收;
(4)根据化学方程式进行计算.
解答 解:(1)氯气不能使干燥的有色布条褪色,干燥的氯气没有漂白性,氯气能使湿润的有色布条褪色,因为氯气和水反应生成的次氯酸具有漂白性,原理方程式为:Cl2+H2O=HCl+HClO,
故答案为:Cl2+H2O=HCl+HClO;干燥的氯气没有漂白性,湿润的氯气具有漂白性;
(2)氯气和水反应的产物是盐酸和次氯酸,要证明谁有漂白性,得做两个实验:证明盐酸是否有漂白性和证明次氯酸是否有漂白性的实验,
故答案为:证明盐酸是否有漂白性;
(3)氯气有毒,会造成空气污染,可以用氢氧化钠来吸收,反应生成氯化钠、次氯酸钠和水,
故答案为:吸收多余的氯气;Cl2+2NaOH=NaCl+NaClO+H2O;
(4)4分钟时n(Cl2)=$\frac{1.12L×4}{22.4L/mol}$=0.2mol,根据反应方程式Cl2+2HaOH=NaCl+NaClO+H2O可知,
需要n(NaOH)=0.4mol,
所以V(NaOH)=$\frac{0.4mol}{2mol/L}$=0.2L=200mL,
故答案为:200.
点评 本题考查HClO的漂白性的探究,题目难度不大,本题注意氯气与次氯酸性质的差异性,注意相关反应化学方程式或者离子方程式的书写.


科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖 | B. | 甘油 | C. | 氨基酸 | D. | 蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌为正极,被氧化 | |
| B. | Ag2O为正极、发生还原反应 | |
| C. | 原电池工作时,电子从Ag2O极经外电路流向锌极 | |
| D. | 原电池工作时,负极附近溶液的p H值增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元).晶体中氧的化合价可看作是部分为0价,部分为-2价.
如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元).晶体中氧的化合价可看作是部分为0价,部分为-2价.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏水 | B. | 氢氧化纳溶液和蒸馏水 | ||
| C. | 盐酸和蒸馏水 | D. | 食盐水和蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键比范德华力强,所以它属于化学键 | |
| B. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| C. | HF分子内存在氢键 | |
| D. | H2O是一种稳定的化合物,这是由于H2O之间形成氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com