
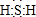 .
.
分析 (1)X为H2S,S最外层6个电子,能够与2个H原子形成共价键;
(2)Na2S2O3中S为+2价,从氧化还原的角度分析,反应物中S元素化合价必须分别大于2和小于2;
(3)①同主族非金属氢化物稳定性减弱,原子半径增大H-Se键的键能小于H-S键的键能;
②依据二氧化硒是酸性氧化物和碱反应生成盐和水.
解答 解:(1)X为H2S,S最外层6个电子,能够与2个H原子形成共价键,其电子式为: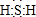 ,故答案为:
,故答案为: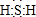 ;
;
(2)Na2S2O3中S为+2价,从氧化还原的角度分析,反应物中S元素化合价必须分别大于2和小于2,a中S化合价都小于2,c中S的化合价都大于2,b符合题意,
故答案为:b;
(3)①同主族非金属氢化物稳定性减弱,原子半径增大H-Se键的键能小于H-S键的键能断开1mol H-Se键吸收的能量比断开1mol H-S键吸收的能量少,用原子结构解释原因:同主族元素最外层电子数相同,从上到下电子层数增加,原子半径增大,原子核对最外层电子的吸引力减弱,元素的非金属性减弱,
故答案为:弱;少;电子层数增加,原子半径增大,原子核对最外层电子的吸引力减弱,元素的非金属性减弱;
②二氧化硒是酸性氧化物和碱反应生成盐和水,反应的离子方程式为:SeO2+2OH-=SeO32-+H2O,
故答案为:SeO2+2OH-=SeO32-+H2O.
点评 本题考查了核外电子的排布与电子式、氧化还原反应,周期表中通主族递变规律的分析应用,掌握基础是关键,题目难度中等.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ②④⑥ | C. | ①③⑥ | D. | ③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.01mol/L的盐酸与0.01 mol/L的NaOH溶液等体积混合后,溶液呈中性 | |
| B. | 0.01mol/L的醋酸与0.01 mol/L的NaOH溶液等体积混合后,溶液呈酸性 | |
| C. | pH=2的盐酸与pH=12的氨水溶液等体积混合后,溶液呈碱性 | |
| D. | pH=2的醋酸与pH=12的NaOH溶液等体积混合后,溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
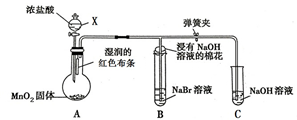 如图是一个制取氯气并验证氯气某些性质的装置.(夹持和加热装置省略)
如图是一个制取氯气并验证氯气某些性质的装置.(夹持和加热装置省略)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com